
����Ŀ��ʵ���⣺�̷���FeSO4��7H2O��������ȱ����ƶѪҩƷ����Ҫ�ɷ֡���������������м��������������������������Ϊԭ�����������̷���һ�ַ�����

��֪�������±��� H2S��Һ�� pH ԼΪ3.9��SnS������ȫʱ��Һ�� pH Ϊ1.6��FeS��ʼ����ʱ��Һ�� pH Ϊ3.0��������ȫʱ�� pH Ϊ5.5��
��1�� ������������Һ���������ữ�� pH��2��Ŀ����_______________________��
��2����������˳������Ϊ________��________�����ˡ�ϴ�ӡ����
��3���������õ����̷�������������ˮϴ�ӣ���Ŀ������
����ȥ������渽�ŵ���������ʣ�
��________________________________________________________________________��
��4���ⶨ�̷���Ʒ��Fe2�������ķ�����
a����ȡһ���������̷���Ʒ�����Ƴ�250.00 mL��Һ��
b����ȡ25.00 mL ������Һ����ƿ�У�
c���������ữ�� 0.010 00 mol��L��1 KMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ20.00 mL��
�ζ�ʱ������Ӧ�����ӷ���ʽΪ5Fe2����MnO4����8H��===5Fe3����Mn2����4H2O
���������ữ�� 0.010 00 mol��L��1 KMnO4��Һ�ζ�ʱ�����ְ�����ʽ�ζ��ܵĻ���������ҡ����ƿ���۾�ע����ƿ����Һ��ɫ�ı仯�жϴ˵ζ�ʵ��ﵽ�յ�ķ�����___________________��
���������������ⶨ����Ʒ��FeSO4��7H2O����������ƫ�����ⶨ�����в��������ɺ������������ԭ����___ _��
���𰸡���1��ʹ Sn2��������ȫ����ֹ Fe2�����ɳ��� ��2������Ũ�� ��ȴ�ᾧ
��3������ϴ�ӹ����� FeSO4��7H2O�����
��4�����μ����һ��KMnO4��Һ����Һ���dz��ɫ�Ұ�����ڲ���ɫ
����Ʒ�д������������ʻ���Ʒ���ֱ�����
��������
�����������1������������Һ���������ữ��pH=2��Ŀ���ǣ�����ҺPH=2ʱ��Sn2+��ȫ�������������Ӳ�������
��2����Һ�еõ����壬��Ҫ����Һ���м�������Ũ�����ᾧ����������ϴ�ӵȣ����Բ���IV��˳������Ϊ���������ᾧ�����ˡ�ϴ�ӣ�
��3����ˮ�¶ȵͣ������ܽ�ȼ�С������ϴȥ����������������ӣ������̷��ܽ��������ʧ��
��4�����ζ�ʵ��ﵽ�յ�ʱ���μ����һ��KMnO4��Һʱ����Һ���dz��ɫ�Ұ�����ڲ���ɫ��
��+2����������������Ʒ�ױ��ʣ����²ⶨ���ƫ�ͣ������Ʒ�к����������ʣ�Ҳ�ܵ��²ⶨ���ƫ�͡�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤��������ֵ������˵����ȷ���� �� ��
A��4.6g��NO2��N2O4��ɵĻ��������ԭ������Ϊ0.2NA
B����״���£�22.4L��SO3�к�3NA����ԭ�ӡ�
C��100mL18.4mol/L��Ũ������������ͭ���ȷ�Ӧ��ת�Ƶĵ�����Ϊ1.84NA
D���ܱյ������У�����������0.5molN2��1.5molH2��Ӧ��õ�NH3������һ��ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ȼ��������۵�674�桢�е�1023�棻���Ȼ�����300��������������������ˮ������ǿ�ҵ���ˮ�ԡ���500���������Ȼ��������������ܷ������ַ�Ӧ����Ӧ֮һΪ��12FeCl2 +3O2![]() 2Fe2O3 +8FeCl3��ij�о�С��ѡ������װ�ã��г�װ��ʡ�ԣ�װ�ÿ��ظ�ѡ�ã����з�Ӧ��̽�����ش��������⣺
2Fe2O3 +8FeCl3��ij�о�С��ѡ������װ�ã��г�װ��ʡ�ԣ�װ�ÿ��ظ�ѡ�ã����з�Ӧ��̽�����ش��������⣺


��1��װ�õĺ�������˳��ΪA�� ��D������Eװ��U�ι�������Ϊ�ֵ��ܵ�Ŀ���� ��
��2��Aװ���з�����Ӧ�Ļ�ѧ����ʽΪ ��
��3����Ӧ���̷��֣�װ��B�г����ɺ���ɫ�����⣬���۲쵽����ɫ���壬���ɸ�����Ļ�ѧ����ʽΪ ��
��4����B�г�ַ�Ӧ��ֹͣ���Ⱥ������ͨ������ ��
��5�����ʵ�飺
������Eװ��U�ι���Ĺ�����֤Fe(OH)3����� ��
�ڲⶨװ��B�IJ�����������Ԫ�ص����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ������������ֵ�������й�������ȷ�ĸ���Ϊ
��1mol����ϩ�к��е�̼̼˫����Ϊ4NA
��4.2g��ϩ�ͱ�ϩ������к��еļ��Լ���ĿΪ0.6NA
�۱���£�3.36LHF���еĵ�����Ϊ1.5NA
�ܳ�����1L 0.5mol/L NH4Cl��Һ��2L 0.25mol/L NH4Cl��Һ����NH4+����Ŀ��ͬ
�ݳ�����4.6gNO2��N2O4�������������ԭ������Ϊ0.3NA
����KClO3+6HCl(Ũ)=KCl+3Cl2+3H2O��Ӧ�У�ÿ����1mol Cl2ת�Ƶĵ�������Ϊ2 NA
��1mol������1mol�����г��ȼ�գ�ʧȥ�ĵ�����Ϊ3NA
������£�16.8g Fe������ˮ������ȫ��Ӧʧȥ0.8NA�����ӣ�
A��3�� B��4�� C��5�� D��6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ֶ�����Ԫ�� A��B��C��D������ A��B��C �����ڱ���������λ����ͼ��ʾ�������ǵ�������֮��Ϊ 32��D Ԫ��ԭ�ӵ�����������Ϊ������������ 2 ����������˵����ȷ���ǣ� ��

A. Ԫ��D�γɵ���̬�⻯��Ŀռ�ṹһ������������
B. A��B ����Ԫ�ص���̬�⻯����ܲ����ǵ�����������Ӧ��ˮ�������Ӧ���ҷ�Ӧ������ͬ
C. DB2��DC4��ÿ��ԭ�Ӷ�����8�����ȶ��ṹ
D. ����Ԫ���γɵ���̬�⻯���У�CԪ���γɵ��⻯����ȶ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���þ����з�̪��Һ���Ȼ�����Һ����ֽ�ֱ������ס�������װ�á�����������ȷ������ ��

A����ֽ�ϵ������Ӷ���̼��Ǩ��
B��a��d�����ĵ缫��Ӧʽ��ͬ
C��b��d������������Һ�����
D��c��d�������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ�{���ӻ�����֪ʶ�ش�����������

��1���ϳɾ۱�ϩ���Ƶĵ���Ľṹ��ʽ�� ����Ӧ������
��2���ϳɵ��������ֵ����������ܺ�NaHCO3��Ӧ�ĵ���Ľṹ��ʽ�� ����˴Ź������ķ�������� ��
��3�����ϳɷ�ȩ��֬��Ҫ���ֵ��壬д�������ֵ���Ľṹ��ʽ ��
��![]() ����ȩ������������Ҳ���Է����������Ʊ���ȩ��֬�ķ�Ӧ������Ӧ�Ļ�ѧ����ʽ�� ��
����ȩ������������Ҳ���Է����������Ʊ���ȩ��֬�ķ�Ӧ������Ӧ�Ļ�ѧ����ʽ�� ��
��4����1,3����������Ա�������Ϊԭ����һ�������ºϳɾ����Ļ�ѧ����ʽΪ ��
��5�� ��NaOH��Һ��һ�������·�Ӧ���÷�Ӧ��ѧ����ʽΪ______��
��NaOH��Һ��һ�������·�Ӧ���÷�Ӧ��ѧ����ʽΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��п�̸ɵ����һ��һ�ε�أ����Ϊ����п���м���̼��������Χ��̼�ۣ��������̣��Ȼ�п���Ȼ�淋���ɵ������õ���ڷŵ���̲���MnOOH��������ˮ�������մ����÷ϵ�ؿ��Եõ����ֻ���ԭ�ϣ��й�������ͼ��ʾ��
�ܽ��/(g/100gˮ)
�¶�/�� ������ | 0 | 20 | 40 | 60 | 80 | 100 |
NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
������ | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp����ֵ | 10-17 | 10-17 | 10-39 |
�ش��������⣺
����ͨп�̵�طŵ�ʱ��������Ҫ��ӦΪ��Zn+2NH4Cl+2MnO2��Zn(NH3)2Cl2+2MnOOH���õ���У�����������Ҫ��________��������������Ҫ��Ӧʽ�� ��
�Ӽ������ҺpH��ʹ��Һ������������Ũ�ȴﵽ mol/L�����պ���ȫ����������Ũ��С��1��10-5mol/Lʱ��������Ϊ�����ӳ�����ȫ���������Ӽ����pHΪ ��п��ʼ�������ٶ�Zn2��Ũ��Ϊ0.1mol/L����
��2���ڷ�����ѧ�г���Na2C2O4��������Һ��ɫ����Ϊ�����ʲⶨKMnO4��Һ��Ũ�ȡ���H2SO4��Һ�У���Ӧ���£�2MnO��5C2O��16H��![]() 2Mn2������Һ��ɫ����10CO2����8H2O��
2Mn2������Һ��ɫ����10CO2����8H2O��
������W g Na2C2O4���100 mL����Һ����ȡ20.00 mL������ƿ�У�������KMnO4��ҺӦװ��__________(���ʽ����ʽ��)�ζ����С����εζ� ѡ��ָʾ����������Ҫ����������Ҫ�������жϵζ����յ��������____ ___��
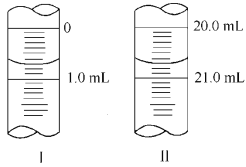
�����ζ�����ʼ�������յ������ͼ��ʾ��������KMnO4�����ʵ���Ũ��Ϊ_ (�����ʽ)��
�����ζ���������������ⶨ��KMnO4��Һ��Ũ��___(�ƫ�ߡ�����ƫ�͡����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ������г���NO2����һ�������½��з�Ӧ��2NO2![]() 2NO+O2���ﵽƽ��״̬�ı�־��
2NO+O2���ﵽƽ��״̬�ı�־��
A��NO2������������NO�������������
B��������NO2�����ʵ�����NO�����ʵ������
C��NO2��O2����������֮��Ϊ2��1
D����λʱ��������2n mol NO��ͬʱ����n mol O2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com