
【题目】下列有机物的命名正确的是
A.CH3CH2CH(CH3)CH(CH3)OH :3-甲基-2-戊醇
B.CH3CH(CH3)CH=CH2:3-甲基丁烯
C.CH3CH2C(CH3)2CH3:2,2-甲基丁烷
D.CH2Cl-CH2Cl:二氯乙烷
科目:高中化学 来源: 题型:
【题目】某温度时,在容积为3 L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析:
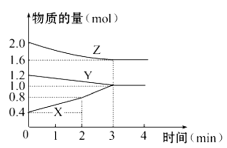
(1)该反应的化学方程式为____________ _______。
(2)反应开始至2 min末,X的反应速率为_____ ____。
(3)该反应是由__________(填序号)开始的。
①正反应 ②逆反应 ③正、逆反应同时
(4)若增加Y的用量,化学反应速率不变化,则Y为__ ___态。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验方法。回答下列问题:
(一)碳酸钙的制备
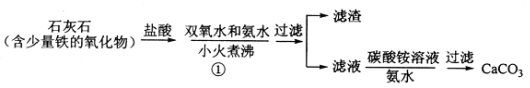
(1)步骤①加入氨水的目的是_______。小火煮沸的作用是使沉淀颗粒长大,有利于____。
(2)下图是某学生的过滤操作示意图,其操作不规范的是______(填标号)。
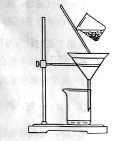
a.漏斗末端颈尖未紧靠烧杯壁
b.玻璃棒用作引流
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(二)过氧化钙的制备
CaCO3![]() 滤液
滤液![]()
![]() 白色晶体
白色晶体
(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈____性(填“酸”、“碱”或“中”。将溶液煮沸,趁热过滤。将溶液煮沸的作用是___________。
(4)步骤③中反应的化学方程式为________,该反应需要在冰浴下进行,原因是_________。
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是_______。
(6)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。该工艺方法的优点是______,产品的缺点是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg/L,我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg/L。某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO。
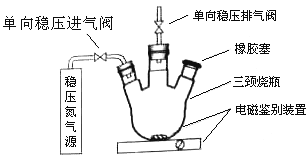
1、测定原理:
碱性体积下,O2将Mn2+氧化为MnO(OH)2:①2Mn2++O2+4OH-=2 MnO(OH)2↓,酸性条件下,MnO(OH)2将I-氧化为I2:②MnO(OH)2+I-+H+→Mn2++I2+H2O(未配平),用Na2S2O3标准溶液滴定生成的I2,③2S2O32-+I2=S4O62-+2I-
2、测定步骤
a.安装装置,检验气密性,充N2排尽空气后,停止充N2。
b.向烧瓶中加入200ml水样
c.向烧瓶中依次迅速加入1mlMnSO4无氧溶液(过量)2ml碱性KI无氧溶液(过量),开启搅拌器,至反应①完全。
d搅拌并向烧瓶中加入2ml硫酸无氧溶液至反应②完全,溶液为中性或若酸性。
e.从烧瓶中取出40.00ml溶液,以淀粉作指示剂,用0.001000mol/L Na2S2O3溶液进行滴定,记录数据。
f.……
g.处理数据(忽略氧气从水样中的溢出量和加入试剂后水样体积的变化)。
回答下列问题:
(1)配置以上无氧溶液时,除去所用溶剂水中氧的简单操作为__________。
(2)在橡胶塞处加入水样及有关试剂应选择的仪器为__________。
①滴定管②注射器③量筒
(3)搅拌的作用是__________。
(4)配平反应②的方程式,其化学计量数依次为__________。
(5)步骤f为__________。
(6)步骤e中达到滴定终点的标志为__________。若某次滴定消耗Na2S2O3溶液4.50ml,水样的DO=__________mg/L(保留一位小数)。作为饮用水源,此次测得DO是否达标:__________(填是或否)
(7)步骤d中加入硫酸溶液反应后,若溶液pH过低,滴定时会产生明显的误差,写出产生此误差的原因(用离子方程式表示,至少写出2个)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应
B.油脂都不能使溴的四氯化碳溶液褪色
C.石油分馏、煤的干馏均为物理变化
D.淀粉、蛋白质和天然橡胶均是天然高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组用0.50 mol·L—1NaOH溶液和0.50 mol·L—1硫酸溶液进行中和热的测定。
I.配制0.50 mol/L NaOH溶液
(1)若实验中大约要使用245 mLNaOH溶液,至少需要称量NaOH固体 g。
(2)从下图中选择称量NaOH固体所需要的仪器是__________(填字母):
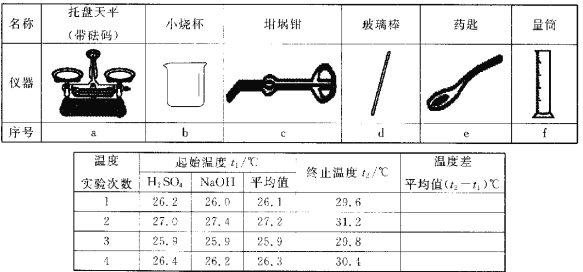
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
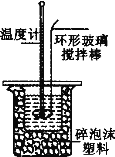
(3)取50 mI。NaOH溶液和30 mL硫酸溶液进行实验,实验数据如上表。
①上表中的温度差平均值为 ℃;
②近似认为0.50 mol/L NaOH溶液和O.50mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),则中和热△H (取小数点后一位)。
③上述实验数值结果与57.3 kJ·mol叫有偏差,产生偏差的原因可能是——(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H。SO。溶液的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com