
【题目】(1)现有下列五种物质A.食盐, B.食醋,C.苹果汁,D.葡萄糖,E.青霉素,请按下列要求填空(填序号)。
富含维生素C的是____;可直接进入血液,补充能量的是___ ;应用最广泛的抗生素之一的是____;即可作为调味剂,又可作为防腐剂、着色剂的是____;食用过多会引起血压升高、肾脏受损的____。
(2)已知维生素A1的键线式如下,线的交点与端点处代表碳原子,并用氢原子补足四价,但C、H原子未标记出来。

回答下列问题:
①维生素A是一类重要的维生素,又称视黄醇,它属于_____(填“水溶性”或“脂溶性”)维生素;如果人体内缺少维生素A,易患_____等眼疾(任写一种), 维生素A含量较高的蔬菜有______。
②维生素A1的结构简式如上图,推测它____使溴水褪色(填“能”或“否”),若1mol维生素A1分子最多可跟_____mol H2发生加成反应。
(3)保持洁净安全的生存环境已成为全人类的共识。
①为了改善空气质量,必须控制大气中二氧化硫、氮氧化物、烟尘等污染物的排放量。为控制大气中二氧化硫的排放,常采取的措施是对化石燃料进行______。对汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,该反应的化学方程式为______。
②获得洁净安全的饮用水是每个人的正常需要。某农村地区为获得饮用水,在将地表水取回家后,常使用漂白粉或漂白精片进行杀菌消毒,其原理可用化学方程式表示为_______。
③人类产生的垃圾应进行分类回收、集中处理,即便如此,仍会剩余不少垃圾,因此必须对剩余垃圾进一步处理,除卫生填埋外,还有一种能够改变垃圾的组成、结构使其体积减小、充分利用其所具有的能量并使之无害化的处理方式,这种垃圾的处理方式是_____技术。
【答案】C D E B A 脂溶性 夜盲症或干眼症 胡萝卜 能 5 脱硫处理 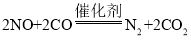 Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO 垃圾焚烧发电
Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO 垃圾焚烧发电
【解析】
(1)依据人体基本营养物质与用途作答;
(2)①维生素A是脂溶性维生素,缺乏会患夜盲症,胡萝卜富含维生素A;
②根据分子的结构简式可知,分子内含碳碳双键,一个碳碳双键可与一个氢气发生加成反应;
(3)①可在煤中添加石灰石进行脱硫处理,汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,生成N2和CO2;
②漂白粉与空气接触后,会和二氧化碳水反应生成碳酸钙和次氯酸,次氯酸具有强氧化性,能进行杀菌消毒漂白;
③充分利用其所具有的能量并使之无害化的处理方式,可将热能转化为电能。
(1)果汁中含维生素C;葡萄糖为营养物质,可直接进入血液补充能量;青霉素为常用的抗生素药物;醋既可作为着色剂,又可作为防腐剂;食盐食用过多会引起血压升高、肾脏受损;
(2)①维生素A是脂溶性维生素,缺乏会患夜盲症或干眼症,胡萝卜、番茄等富含维生素A;
②维生素A分子内含碳碳双键,可使溴水褪色,1个该分子内含5个碳碳双键,故1mol维生素A1分子最多可跟5mol H2发生加成反应;
(3)①可在煤中添加石灰石进行脱硫处理,生成硫酸钙,汽车加装尾气催化净化装置,使其中的有害气体NO、CO转化为无害气体,生成N2和CO2,反应的方程式为: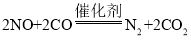 ;
;
(2)碳酸酸性强于次氯酸,漂白粉与空气接触后,会和二氧化碳水反应生成碳酸钙和次氯酸,次氯酸具有强氧化性,能进行杀菌消毒漂白,反应的化学方程式为:Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO;
(3)充分利用其所具有的能量并使之无害化的处理方式,可将热能转化为电能,该技术为垃圾焚烧发电技术。


科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
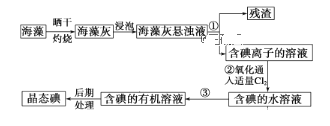
(1)指出提取碘的过程中①的实验操作名称_________及玻璃仪器名称______________________________________。
(2)写出过程②中有关反应的离子方程式:_____________________。
(3)操作③的名称_____________,用到的主要仪器_____________。
(4)提取碘的过程中,可供选择的有机试剂是(______)。
A.酒精 B.四氯化碳 C.甘油 D.醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是

A. 甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙
B. 生成1mol H2O时吸收热量245kJ
C. H2O分解为H2与O2时放出热量
D. 氢气和氧气的总能量小于水的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
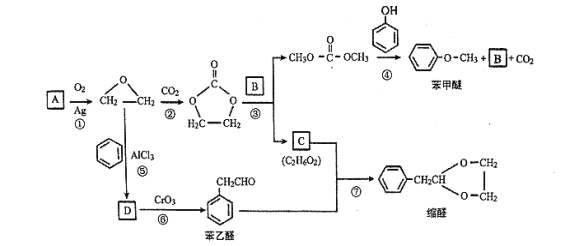
【题目】A (C2H4)是基本的有机化工原料。用A和常见的有机物可合成一种醚类香料和一种缩醛类香料,具体合成路线如图所示(部分反应条件略去):
已知:![]()
回答下列问题:
(1)B的分子式是_______,C中含有的官能团名称是_______。
(2)若D为单取代芳香族化合物且能与金属钠反应;每个D分子中只含有1个氧原子, D中氧元素的质量分数约为13.1%,则D的结构简式为_______,⑥的反应类型是_______。
(3)据报道,反应⑦在微波辐射下,以NaHSO4·H2O为催化剂进行,请写出此反应的化学方程式:_______。
(4)请写出满足下列条件的苯乙醛的所有同分异构体的结构简式:_______。
i .含有苯环和结构![]()
ii.核磁共振氢谱有4组峰,且峰面积之比为3 : 2 : 2 : 1
(5)若化合物E为苯甲醚的同系物,且相对分子质量比苯甲醚大14,则能使FeCl3溶液显色的E的所有同分异构体共有_______ (不考虑立体异构)种。
(6)参照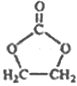 的合成路线,写出由2-氯丙烷和必要的无机试剂制备
的合成路线,写出由2-氯丙烷和必要的无机试剂制备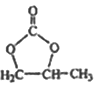 的合成流程图:_______。
的合成流程图:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述正确的是
A. 常温常压下,30g乙烷气体中所含有的共价键数目为6NA
B. 常温下,100mL0.1mol/L NH4Cl溶液中含有NH4+数目为0.01NA
C. 1molFe分别与足量的稀硫酸和稀硝酸反应转移电子数均为2 NA
D. 0.1molH2和0.1molI2于密闭容器中充分反应后,其分子总数为0.2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL含HCl的AlCl3溶液中逐滴加入0.1mol·L-1的NaOH溶液,加入NaOH溶液的体积V(mL)与产生Al(OH)3沉淀的物质的量n(mol)的关系如图:

试计算:(请写出运算过程)
(1)原溶液中HCl的物质的量浓度。____________
(2)原溶液中AlCl3的物质的量浓度。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:如图中A是金属铁,请根据图中所示的转化关系,回答下列问题:

(1)写出E的化学式 ____;
(2)写出反应③的化学方程式:__________ ;
(3)写出①④在溶液中反应的离子方程式:________、 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来“雾霾”污染日益严重,原因之一是机动车尾气中含有NO、NO2、CO等气体,火力发电厂释放出大量的NOx、SO2和CO2等气体也是其原因,现在对其中的一些气体进行了一定的研究:
(1)用 CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:①CH4(g) + 4NO2(g) = 4NO(g) + CO2(g) + 2H2O(g) △H = - 574 kJ/mol
②CH4(g) + 4NO(g) = 2N2(g) + CO2(g) + 2H2O(g) △H = - 1160 kJ/mol
③H2O(g) = H2O(l) △H = - 44.0 kJ/mol
写出 CH4(g)与 NO2(g)反应生成 N2(g)、CO2(g)和 H2O(l)的热化学方程式: _____________________________________________________________。
(2)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体。4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是________________(填代号)。

(3)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH=a kJ/mol
N2(g)+CO2(g) ΔH=a kJ/mol
在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(NO)=_____________________;计算该反应的平衡常数K=____________________。
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是_________(填字母代号)。
A.通入一定量的CO2 B.加入合适的催化剂
C.适当缩小容器的体积 D.通入一定量的NO
E.加入一定量的活性炭
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为2:1:1,则达到新平衡时NO的转化率____________(填“升高”或“降低”),a________0(填“>”或“<”)。
(4)温度T1和T2时,分别将0.50 mol CH4和1.2mol NO2充入1 L的密闭容器中发生反应:CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g) △H=bkJ/mol。
N2(g)+CO2(g)+2H2O(g) △H=bkJ/mol。
测得有关数据如下表:
温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
下列说法正确的是__________________。
A.T1>T2,且b>0
B.当温度为T2、反应进行到40 min时, x>0.15
C.温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)<0.70mol
D.温度为T1时,若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50molH2O(g),反应开始时,ν(正)>ν(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
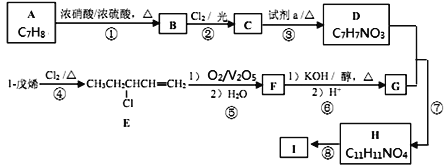
【题目】功能高分子I的一种合成路线如下,其中D能与Na反应生成H2,且D苯环上的一氯代物有2种。
已知:![]()
回答下列问题:
(1)A的名称为________,试剂a为________________。
(2)C的结构简式为________________________。
(3)F中的官能团名称为________。
(4)上述①—⑧的反应中,不属于取代反应的是________(填数字编号)。写出反应⑦的化学方程式________________________________________。
(5)符合下列条件的B的同分异构体有________种。
①苯环上有氨基(—NH2) ②能发生银镜反应
其中核磁共振氢谱有4组峰,且峰面积比为2∶2∶2∶1的结构简式为__________。
(6)参照上述合成路线,以1-丁烯为原料(无机试剂任选),设计制备丙烯酸(CH2=CHCOOH)的合成路线________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com