
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是( )
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1:1
D.第二次平衡时,Z的浓度为0.4 mol·L-1
【答案】D
【解析】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),则可等效为两等效平衡体系合,在合并瞬间X、Y、Z的体积分数不变,但单位体积内体系分子总数增多,依据勒夏特列原理平衡应朝使单位体积内分子总数减小方向移动,但再次达到平衡后,X、Y、Z的体积分数不变,则说明m+1=3,故m=2,A项正确;同一化学反应的平衡常数只与温度有关,两次平衡温度不变,故两次平衡的平衡常数相同,B项正确;m=2,则起始量X与Y之比为1:2,则反应过程中由方程式可知反应的X与Y之比为1:2,故X与Y的平衡转化率之比为1:1,C项正确;m=2,则该反应为反应前后气体总量不变的反应,故第二次平衡时Z的物质的量为:4×10%=0.4mol,故Z的浓度为0.4mol÷2L=0.2mol/L,故D项错误;本题选D。
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),则可等效为两等效平衡体系合,在合并瞬间X、Y、Z的体积分数不变,但单位体积内体系分子总数增多,依据勒夏特列原理平衡应朝使单位体积内分子总数减小方向移动,但再次达到平衡后,X、Y、Z的体积分数不变,则说明m+1=3,故m=2,A项正确;同一化学反应的平衡常数只与温度有关,两次平衡温度不变,故两次平衡的平衡常数相同,B项正确;m=2,则起始量X与Y之比为1:2,则反应过程中由方程式可知反应的X与Y之比为1:2,故X与Y的平衡转化率之比为1:1,C项正确;m=2,则该反应为反应前后气体总量不变的反应,故第二次平衡时Z的物质的量为:4×10%=0.4mol,故Z的浓度为0.4mol÷2L=0.2mol/L,故D项错误;本题选D。


科目:高中化学 来源: 题型:
【题目】X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X(g)+2Y(g)![]() 2Z(g),达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
2Z(g),达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
A.33% B.40% C.50% D.65%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关垃圾处理的方法不正确的是:
A. 垃圾处理常用的方法是卫生填埋、焚烧、堆肥
B. 将垃圾分类回收是垃圾处理的发展方向
C. 填埋垃圾不需处理,只深埋即可
D. 焚烧垃圾产生大量污染空气的物质,故不易采用此方法
查看答案和解析>>
科目:高中化学 来源: 题型:
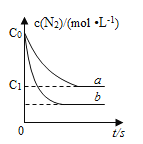
【题目】汽车尾气中,产生NO的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是( )
A.温度T下,该反应的平衡常数K=![]()
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人们生活节奏的加快,方便的袋装食品已被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,常在袋装食品内放入一小袋固体,在该小袋中应 放入的化学物质是 ( )
A. 无水硫酸铜、蔗糖 B. 生石灰、硫酸亚铁 C. 食盐、硫酸亚铁 D. 生石灰、食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应速率与限度与生产、生活密切相关
(1)A学生为了探究锌与盐酸反应过程中的速率变化,他在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
①反应速率最大的时间段是(指0~1、1~2、2~3、3~4、4~5 )____min,原因是_________________。
②求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率________________。(设溶液体积不变)
(2)B学生也做同样的实验,但由于反应太快,测不准氢气体积,故想办法降低反应速率,请你帮他选择在盐酸中加入下列__________以减慢反应速率。(填写代号)
A.蒸馏水 B.冰块 C.HNO3溶液 D.CuSO4溶液
(3)某温度下在10L密闭容器中,3种气态物质A、B、C的物质的量随时间变化曲线如图。

①该反应的化学方程式是________。
②求在该条件达到反应的限度(平衡状态)时反应物的转化率【转化率=(转化的物质的量/初始物质的量)×100%】,请写出计算过程,计算结果保留1位小数)________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述错误的是
A. 分子总数为NA的NO2和CO2的混合气体中含有的氧原子数为2 NA
B. 0.1 mol/L (NH4)2SO4溶液与0.2 mol/L NH4Cl溶液中的NH4+数目相同
C. 标准状况下,H2和CO混合气体8.96 L在足量O2中充分燃烧消耗O2分子数为0.2 NA
D. 1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在陶瓷器皿表面的釉质中含有极微量的Pb、Cd、Sb等有毒金属盐类,为防止中毒,不能长期盛放下列物质的是( )
A. 食盐 B. 酱油
C. 蔗糖 D. 食醋
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.SO2、CO2、SiO2中的S、C、Si均为sp3杂化
B.H3O+、NH4+、[Cu(NH3)4]2+均含有配位键
C.SO32—、CO32—、SiO32—均为平面三角形
D.石墨、新型高分子导电材料、聚乙烯、金属晶体均含有金属键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com