
����Ŀ����ѧ��Ӧ���������������������������
��1��Aѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������200mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
���������mL������״���� | 100 | 240 | 464 | 576 | 620 |
�ٷ�Ӧ��������ʱ����ǣ�ָ0��1��1��2��2��3��3��4��4��5 ��____min��ԭ����_________________��
����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����________________��������Һ������䣩
��2��Bѧ��Ҳ��ͬ����ʵ�飬�����ڷ�Ӧ̫�죬�ⲻ�������������취���ͷ�Ӧ���ʣ��������ѡ���������м�������__________�Լ�����Ӧ���ʡ�����д���ţ�
A������ˮ B������ C��HNO3��Һ D��CuSO4��Һ
��3��ij�¶�����10L�ܱ������У�3����̬����A��B��C�����ʵ�����ʱ��仯������ͼ��

�ٸ÷�Ӧ�Ļ�ѧ����ʽ��________��
�����ڸ������ﵽ��Ӧ���ȣ�ƽ��״̬��ʱ��Ӧ���ת���ʡ�ת����=��ת�������ʵ���/��ʼ���ʵ�������100%������д��������̣�����������1λС����________
���𰸡� 2��3 ��÷�Ӧ���ȣ����ŷ�Ӧ����Һ�¶����ߣ��ʷ�Ӧ���ʼӿ� 0.1 mol/Lmin AB��2�֣� 2C ![]() A +3B ת����=66.7% ��������̵�1�֣����̺�����������ȷ��2����
A +3B ת����=66.7% ��������̵�1�֣����̺�����������ȷ��2����
�����������������������Ҫ����Ӱ����Ӧ���ʵ����ؼ���Ӧ���ʵļ��㡣
(1)����Ӧ��������ʱ�����2��3min��ԭ������÷�Ӧ���ȣ����ŷ�Ӧ��Һ�¶����ߣ��ʷ�Ӧ���ʼӿ졣
��2��3����ʱ����������������ʵ���Ϊn=![]() =
=![]() =0.01mol������HCl0.02mol���������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����Ϊ(0.02/0.2) mol/Lmin =0.1 mol/Lmin ��
=0.01mol������HCl0.02mol���������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����Ϊ(0.02/0.2) mol/Lmin =0.1 mol/Lmin ��
��2��A.ϡ�ͣ�����Ũ�ȱ�С����Ӧ���ʼ����� B.���£���Ӧ���ʼ����� C.HNO3��Һ����ǿ�����ԣ���п��Ӧ��������������D.п�û�ͭ���γ�ԭ��ؼӿ췴Ӧ���ʡ���ѡAB��
��3��5min������2molC������1molA��3molB�������÷�Ӧ�Ļ�ѧ����ʽ��2C ![]() A +3B ��
A +3B ��
����Ӧ���ת����=2/3=66.7%��


 �����ߴ���ϵ�д�
�����ߴ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ�о���ѧϰС����CO��ԭFe2O3������ʵ��������ô����������ɵĺ�ɫ��ĩX����̽����
[̽��Ŀ��] ������ɫ��ĩX����ɣ����������ʵ�顣
[��������]
I��CO��ԭFe2O3��ʵ�������¶Ȳ�ͬ�����Ȳ���ʱ������Fe3O4��Ҳ�ܱ�����������
II��Fe3O4 �� 8H+ = 2Fe3+ �� Fe2+ �� 4H2O
[�������] ��ɫ��ĩX����ɿ�����_________��_________������ߵĻ���
[ʵ��̽��]
��� | ʵ����� | ʵ������ |
�� | ȡ������ɫ��ĩX�����Թ��У�ע��������һ��Ũ�ȵ����ᣬ�� | ��ɫ��ĩ���ܽ⣬ͬʱ�����ݲ�������Һ��dz��ɫ�� |
�� | �������Թ��еμӼ���KSCN��Һ���� | ��Һû�г��ֺ�ɫ |
��1��ʵ�����в������ݵ����ӷ���ʽΪ_________��
��2������������Һδ�ʺ�ɫ�������ƶϳ���ɫ��ĩX����Fe3O4���������ӷ���ʽ����ԭ��_________��
��3��Ϊ��֤����ɫ��ĩX���Ƿ���Fe3O4����С���������ͼ��ʾʵ�飺
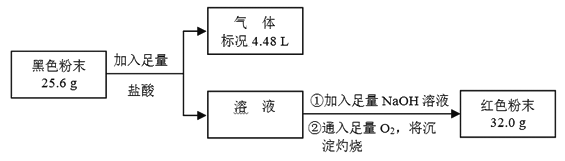
��������ݷ���˵����ɫ��ĩX���Ƿ���Fe3O4��
_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2��Cl2�������������������ˮ�������߱��ʵȷ���Ӧ�ù㷺��ij��ȤС��ͨ����ͼ1װ�����г�װ�����������Ʊ������ա��ͷź�Ӧ�ý������о���

��1������A��������________________����װF�е���ʱ��Ӧѡ��ͼ2�е�_________��
��2����B�Ļ�����A�з�����Ӧ��2NaClO3��4HCl===2ClO2����Cl2����2NaCl��2H2O��ΪʹClO2��D�б��ȶ���������գ��μ�ϡ������ٶ���__________����������������������
��3���ر�B�Ļ�����ClO2��D�б��ȶ�����ȫ��������NaClO2����ʱF����Һ����ɫ���䣬��װ��C��������________________________________��
��4����֪������������NaClO2�ɷ�����Ӧ����NaCl���ͷų�ClO2���÷�Ӧ�����ӷ���ʽΪ_________________________����ClO2�ͷ�ʵ���У���E�Ļ�����D�з�����Ӧ����װ��F��������_________________________________��
��5��������ClO2������ȶ�������ȶ���������ͷ�ClO2��Ũ����ʱ��ı仯��ͼ��ʾ������������ˮ�����ʣ�����ΪЧ���Ϻõ��ȶ�����_____________��

���ɣ�_____________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���һԪ�� HA ����Һ�� KOH ��Һ��������(��������仯)��ʵ���������±���
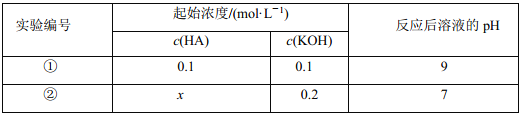
�����жϲ���ȷ����( )
A��ʵ������Ӧ�����Һ�У�c(K+)>c(A��)>c(OH��)>c(H+)
B��ʵ������Ӧ�����Һ�У�c(OH��)��c(K+)��c(A��)��![]()
C��ʵ������Ӧ�����Һ�У�c(A��)+c(HA)>0.1 mol/L
D��ʵ������Ӧ�����Һ�У�c(K+)��c(A��)>c(OH��)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶��£���2L���ܱ������У�����1molX��g����2molY��g��������Ӧ��X��g��+m Y��g��![]() 3Z��g����ƽ��ʱ��X��Y��Z����������ֱ�Ϊ30%��60%��10%���ڴ�ƽ����ϵ�м���1molZ��g�����ٴδﵽƽ���X��Y��Z������������䡣������������ȷ���ǣ� ��
3Z��g����ƽ��ʱ��X��Y��Z����������ֱ�Ϊ30%��60%��10%���ڴ�ƽ����ϵ�м���1molZ��g�����ٴδﵽƽ���X��Y��Z������������䡣������������ȷ���ǣ� ��
A��m=2
B������ƽ���ƽ�ⳣ����ͬ
C��X��Y��ƽ��ת����֮��Ϊ1:1
D���ڶ���ƽ��ʱ��Z��Ũ��Ϊ0.4 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڻ�ѧ����˵����ȷ���ǣ� ��
A.���ɵ��ʷ��ӵ���һ�����й��ۼ�
B.�ɷǽ���Ԫ����ɵĻ����ﲻһ���ǹ��ۻ�����
C.�Ǽ��Լ�ֻ������˫ԭ�ӷ�����
D.���й��ۼ��Ļ����ﶼ�ǹ��ۼ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��R��X��T��Z��Q��Ԫ�����ڱ��е����λ�����±���ʾ�� ����R�����ڰ�����H2���һ��ϲ�������ը���������ж���ȷ����( )
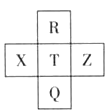
A. T�ĵ����ڻ�ѧ��Ӧ��ֻ����������
B. R��Q�ĵ��������16
C. T�γɵĺ����������һ����X�γɵĺ�����ǿ
D. ��������Ԫ����Z�Ļ�ѧ�������ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ���������ε����Ҷ�С��36��X��Y��Z��Q��W����Ԫ�أ�����X��ԭ�Ӱ뾶��С��Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Qԭ�ӻ�̬ʱ2pԭ�ӹ������2��δ�ɶԵĵ��ӣ�WԪ�ص�ԭ�ӽṹ��3d�ܼ���4��δ�ɶԵ��ӡ��ش��������⣺
��1��Y2X2������Yԭ�ӹ�����ӻ�����Ϊ ��Y2X2����������������������Ϊ ��
��2��������ZX3�ķе�Ȼ�����YX4�ĸߣ�����Ҫԭ���� ��
��3��Ԫ��Y��һ����������Ԫ��Z��һ�������ﻥΪ�ȵ����壬Ԫ��Z������������ķ���ʽ�� ��
��4��Ԫ��W���γɶ��������磺W(CO)5�ȡ�
����̬W3+��M������Ų�ʽΪ ��
��W(CO)5�����³�Һ̬���۵�Ϊ��20.5�����е�Ϊ103���������ڷǼ����ܼ����ݴ˿��ж�W(CO)5�������� ����(�������)���þ�����W�Ļ��ϼ�Ϊ ��
��5�������йص�˵����ȷ���� ��
A�����Ӿ����У����ۼ�����Խ�÷��Ӿ�����۷е�Խ��
B���縺��˳��X��Y��Z��Q
C����Ϊ������CaO��KCl�ߣ�����KCl��CaO�۵��
D��H2 YO3�ķ��ӽṹ�к���һ�����ǻ���������Ϊ��ǿ��
��6��Q��Na�γɵ�һ��ֻ�������Ӽ������ӻ�����ľ����ṹ��ͼ4����һ����������Χ���������������Ϊ���㹹�ɵļ�����Ϊ ����֪�þ����ܶ�Ϊ�� g/cm3�������ӵ�����ΪNA�����߳�a= pm��(�ú�����NA�ļ���ʽ��ʾ)
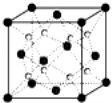
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
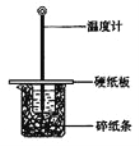
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ��������� ��
��2�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ (�ƫ��ƫС����Ӱ�족)
��3�������60mL0.50mol/L������50mL0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������� (���ȡ�����ȡ�)�������к��ȡ�H_____ (���ȡ�����ȡ�)
��4���������ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬������к��ȡ�H�� (�ƫ����ƫС��������Ӱ�족) ����KOH����NaOH��ʵ�������������_________________(�ƫ����ƫС��������Ӱ�족)��
��5�����Ǽ�¼��ʵ���������£�
ʵ����Ʒ[ | ��Һ�¶� | �к��� ��H | |||
��ʼƽ ���¶� | ��Ӧ����¶� | ||||
�� | 50mL��0.55mol.L-1NaOH | 50mL��0.5mol.L-1HCl | 20�� | 23.3�� | |
�� | 50mL��0.55mol.L-1NaOH | 50mL��0.5mol.L-1HCl | 20�� | 23.5�� | |
��֪��Ӧ����Һ�ı�����CΪ4.18KJ����-1�� Kg-1�������ʵ��ܶȾ���Ϊ1g��cm-3��
�ٸ����ϱ����ݼ����к��ȡ�H=__________(������С�����һλ)
�ڸ���ʵ����д��NaOH��Һ��HCl��Һ��Ӧ���Ȼ�ѧ����ʽ�� ��
��6������ʵ����ֵ�����57.3 kJ/mol��ƫ�����ƫ���ԭ�������(����ĸ)_______________��
A��ʵ��װ�ñ��¡�����Ч����
B����ȡϡ������Һ�����ʱ���Ӷ���
C��һ����NaOH��Һ����ʢ�������С�ձ���
D�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨHCl��Һ���¶�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com