
AD
【解析】
试题分析:A.由于该反应的正反应是吸热反应,所以升高温度,平衡逆向移动,C的含量减小,正确;B.当反应达到平衡后增大压强,反应混合物中的各种物质的浓度都增大,因此正反应、逆反应的速率都加快,错误;C.加入催化剂能够改变反应途径,降低反应的活化能,因此化学反应速率加快,但是不能使平衡发生移动,因此C的平衡浓度不变,错误;D.由于该反应的正反应是气体体积减小的放热反应,所以在其它条件不变时,增大压强,平衡正向移动,A的转化率增大,当压强不变时,升高温度,平衡逆向移动,A的平衡转化率降低,故该选项正确。
考点:考查外界条件对化学反应速率、化学平衡移动、物质的转化率及平衡浓度的影响的知识。


科目:高中化学 来源:2013-2014陕西西安铁一中、铁一中国际合作校高三四月月考化学试卷(解析版) 题型:填空题
(15分)空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
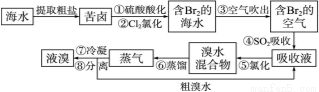
(1)溴在周期表中位于第______周期第________族。
(2)步骤①中用硫酸酸化可提高Cl2的利用率,理由是__________________________。
(3)步骤④利用了SO2的还原性,反应的离子方程式为________________________。
(4)步骤⑥的蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因____________________________________________________。
(5)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是____________。
(6)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是_________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省高一第二学期期末化学试卷(解析版) 题型:填空题
(8分)完成下列方程式(要注明反应条件)。
①甲烷与氯气反应制一氯甲烷:________________________ ②乙烯使溴水褪色:_______________
③苯和液溴混合加铁粉 :__________________④制备乙酸乙酯:_________________________________
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省高一第二学期期末化学试卷(解析版) 题型:选择题
下列叙述不正确的是( )
①NH3易液化,液氨常用作制冷剂
②与金属反应时,稀HNO3可能被还原为更低价态,则稀HNO3氧化性强于浓HNO3
③铵盐受热易分解,因此贮存铵态氮肥时要密封保存,并放在阴凉通风处
④稀HNO3和活泼金属反应时主要得到氢气
A.①③ B.②④ C.①②③④ D.都不正确
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省延安市第一学期期末考试高二化学试卷(解析版) 题型:填空题
(10分)实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下
实验。请你完成下列填空:
步骤一:配制100mL 0.10mol/L NaOH标准溶液。.
步骤二:取20.00mL待测稀盐酸放入锥形瓶中,并滴加2~3滴酚酞溶液作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.10 | 22.02 | 20.00 |
2 | 0.10 | 22.00 | 20.00 |
3 | 0.10 | 21.98 | 20.00 |
(1)滴定达到终点的现象是 ;
此时锥形瓶内溶液的pH的范围是 。
(2)根据上述数据,可计算出该盐酸的浓度为 。
(3)排去碱式滴定管中气泡的方法应采用下图的 操作,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

(4)在上述实验中,下列操作(其他操作正确)会造成测定结果(待测液浓度值)偏高的有 (多选扣分):
A 配制标准溶液定容时,加水超过刻度 B 锥形瓶水洗后直接装待测液
C 酸式滴定管水洗后未用待测稀盐酸溶液润洗 D 滴定到达终点时,仰视读出滴定管读数;
E. 碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省延安市第一学期期末考试高二化学试卷(解析版) 题型:选择题
若醋酸用HAc表示,则在0.1mol·L-1 NaAc溶液中,下列离子浓度关系正确的是
A.c(Na+)= c(Ac—)+c(HAc)
B.c(Na+)+c(OH—)= c(Ac— )+c(H+)
C.c(Na+)>c(OH—) > c(Ac—) > c(H+)
D.c(Na+)> c(Ac—)> c(H+)> c(OH—)
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省延安市下学期期末考高一化学试卷(解析版) 题型:填空题
(8分)将等物质的量的A、B混合于2 L的密闭容器中,发生如下反应: 3A(g)+B(g) xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c (A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c (A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
(1)此时A的浓度c(A)=________mol/L,反应开始前容器中的A、B的物质的量:n(A)= n(B)=________mol;
(2)B的平均反应速率v(B)=________mol/(L·min);
(3)x的值为________。
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省延安市下学期期末考高一化学试卷(解析版) 题型:选择题
下表为元素周期表前四周期的一部分,且X、Y、Z、R和W为主族元素。下列说法正确的是
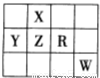
A.五种元素可能都是金属元素
B.五种元素的原子最外层电子数一定都大于2
C.X的氢化物的沸点一定比Z的氢化物的沸点高
D.R的最高价氧化物对应的水化物一定是强酸
查看答案和解析>>
科目:高中化学 来源:2013-2014陕西省岐山县第二学期高一期末化学试卷(解析版) 题型:选择题
在一定温度下的定容容器中,当下列物理量不再发生变化时,不能表明可逆反应
A(g) + 2B(g) C(g) + D(g)(正反应为放热反应)已达到平衡状态的是
C(g) + D(g)(正反应为放热反应)已达到平衡状态的是
A.混合气体的压强 B.混合气体的密度
C.B的物质的量浓度 D.反应放出的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com