
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是
| A.X的气态氢化物比Y的稳定 |
| B.Z的非金属性比Y的强 |
| C.W的最高价氧化物对应水化物的酸性比Z的强 |
| D.X与Y形成的化合物都能与水反应 |
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:单选题
下列各组物质的性质由强到弱的顺序排列正确的是
| A.酸性:HClO4>H3PO4>H2SO4 | B.氢化物稳定性:H2S>HF>H2O |
| C.碱性:NaOH>Al(OH)3>Mg(OH)2 | D.氧化性:F2 > Cl2 > Br2 > I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D、E五种元素原子序数依次增大,且均不超过18。其中A与C、B与E分别为同族元素。原子半径A<B<E<D<C,B原子最外层电子数是内层电子数的3倍,C、D的核外电子数之和与B、E核外电子数之和相等。下列说法正确的是
A.原子最外层电子数:B<A B.A与E形成的化合物是离子化合物
C.最高价氧化物对应的水化物碱性:C<D D.B与E可以形成EB2型化合物
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期主族元素A、B、C、D原子序数依次增大。A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述不正确的是
A.原子半径:B>C>D>A B.单质B制作的容器可用来盛放浓硝酸
C.A、C形成的物质属于两性氧化物 D.元素D在周期表中位于第三周期、VIIA族
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )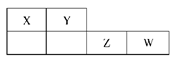
| A.氢化物稳定性:X>Y |
| B.最高价氧化物对应的水化物的酸性:W>Y |
| C.4种元素的单质中,W单质的熔、沸点最高 |
| D.干燥的W单质具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲、乙两种非金属:①甲比乙容易与氢气化合;②甲能与乙的阴离子发生置换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低。能说明甲比乙的非金属性强的是( )
| A.只有④ | B.只有⑤ | C.①②③ | D.①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com