
常温下,下列各组离子在溶液中一定能大量共存的是
A.PH=2的溶液:K+、Na+、CH3COO﹣、CO32﹣
B.与铝反应产生大量氢气的溶液:Mg2+、K+、HCO3﹣、NO3﹣
C.使酚酞呈红色的溶液中:Na+、K+、SiO32﹣、AlO2﹣
D.FeBr2溶液中滴加KI淀粉溶液变为蓝色
科目:高中化学 来源:2016届湖南省衡阳市高三上学期第三次月考化学试卷(解析版) 题型:选择题
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y
B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S
C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料
D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH>Ba(OH)2
查看答案和解析>>
科目:高中化学 来源:2016届河北省邯郸市高三上学期10月月考化学试卷(解析版) 题型:选择题
下列依据热化学方程式得出的结论正确的是
A.已知:2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ·mol-1
B.已知C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定
C.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
D.已知2C(s)+2O2(g)===2CO2(g) ΔH1, 2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1<ΔH2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上学期10月月考化学试卷(解析版) 题型:填空题
(8分)已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表:
醋酸 | 碳酸 | 亚硫酸 |
Ka= 1.75×10-5 | Ka1= 4.30×10-7 Ka2 = 5.61×10-11 | Ka1= 1.54×10-2 Ka2 = 1.02×10-7 |
(1)写出碳酸的第一步电离平衡常数表达式:Ka1 = 。
(2)在相同条件下,试比较H2CO3、HCO3-和HSO3-的酸性强弱: > > 。
(3)下图表示常温时稀释醋酸、碳酸两种酸的稀溶液时,溶液PH随水量的变化
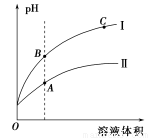
①图像中,曲线I表示的酸是 (填化学式)。
②A、B、C三点中,水的电离程度最大的是 (填字母)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高二上学期10月月考化学试卷(解析版) 题型:选择题
室温下,对PH相等、体积相同的盐酸和醋酸分别进行以下操作,下列说法正确的是
A.将温度迅速升高20℃,两溶液的PH均增大
B.加水稀释相同倍数后,两溶液的PH同等程度减小
C.加少量的醋酸钠固体后,两溶液的PH均增大
D.加足量的锌充分反应后,两溶液产生的氢气的量一样多
查看答案和解析>>
科目:高中化学 来源:2016届福建省四地六校高三上学期第一次联考化学试卷(解析版) 题型:选择题
质量分数为a的某物质的溶液m g与质量分数为b的该物质的溶液n g混合后,蒸发掉p g水,得到的溶液密度为q g/cm3(此过程中无溶质析出),物质的量浓度为c mol·L﹣1.则溶质的相对分子质量为
A.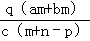 B.
B.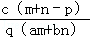
C.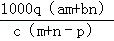 D.
D.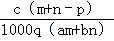
查看答案和解析>>
科目:高中化学 来源:2016届江西省吉安市高三上学期第一次月考化学试卷(解析版) 题型:推断题
A是用途最广的金属,B、C是两种常见气体单质,E溶液为常见强酸,D溶液中滴加KSCN溶液显红色,它们相互转化关系如图所示.
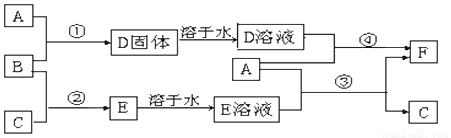
请回答:
(1)写出B物质的化学式: .
(2)写出第③步反应的化学方程式为 .
(3)第④步反应的离子方程式是 .
(4)写出SO2在水中与B反应的离子方程式 .
(5)F溶液中滴入NaOH溶液可能产生的实验现象是 .
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期第一次检测化学试卷(解析版) 题型:实验题
(12分)实验室用固体烧碱配制500 mL 0.1 mol·L―1的NaOH溶液。
(1)需称量____________g的烧碱固体,它应该盛放在____________ 中进行称量。
(2)配制过程中,不需要使用的仪器是(填写代号)_________________。
A.烧杯 B.量筒 C.1000 mL容量瓶 D.托盘天平E.药匙 F.500 mL容量瓶 G.胶头滴管 H.漏斗
除上述可使用的仪器,还缺少的仪器是_________ ,
(4)叙述定容过程中的操作___________________________________。
(5)要配制浓度约为2 mol·L-1 NaOH溶液100 mL,下列操作正确的是_____ 。
①称取8 g NaOH固体,放入250 mL烧杯中,用100 mL量筒量取100 mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解。
②称取8 g NaOH固体,放入100 mL量筒中,边搅拌,边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL。
③称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加水至刻度线,塞好瓶塞,反复摇匀。
④用100 mL量筒量取40 mL 5 mol·L-1 NaOH,倒入250 mL烧杯中,再用同一量筒量取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中。
(6)下列操作导致所配溶液浓度偏高的是
A.称量时,左盘高,右盘低 B.定容时俯视容量瓶刻度线
C.原容量瓶洗净后没有干燥 D.摇匀后见液面下降,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上段中考试化学试卷(解析版) 题型:填空题
Ⅰ(只普通班做学生解答,答错题不给分)(18分)
(1)有下列四组物质①水、酒精、煤、石油 ②CaO、SO3、SO2、P2O5 ③HNO3、H2SO4、HCl、NaCl ④KClO3、KCl、KMnO4、HgO各组中均有一种物质所属类别与其他物质不同,这四种物质分别是:①__________;②______ __;③_______;④__________。
(2)将标准状况下22.4 L的HCl 溶于水配成200 mL的溶液,所得溶液的物质的量浓度为__________mol/L;
(3)3.01×1023个OH-的物质的量为___________mol,质量为___________g,含有电子的物质的量为___________mol,这些OH-与___________mol NH3的质量相同.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com