
| 0.05mol |
| 0.9L |
| 0.05mol×2 |
| 1L |
| 0.05mol×2-0.1mol/L×VL |
| 0.1L+VL |


科目:高中化学 来源: 题型:
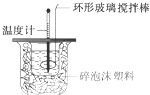 测定稀盐酸和稀氢氧化钠中和热的实验装置如图所示.
测定稀盐酸和稀氢氧化钠中和热的实验装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、14-a+b |
| B、14+a+b |
| C、14-a-b |
| D、14+a-b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化产物是HO2 |
| B、HO2在碱中能稳定存在 |
| C、氧化剂是O2 |
| D、1 mol Cu参加反应有2 mol电子发生转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、可用托盘天平准确称取3.15gNaCl |
| B、实验室中可用燃烧法处理CO、H2、H2S等可燃性尾气 |
| C、测定中和热时,环形玻璃搅拌棒可用铜丝代替或直接用温度计搅拌 |
| D、Fe2+与Fe[(CN)6]3-反应生成Fe3[Fe(CN)6]2蓝色沉淀,该反应可用于Fe2+的检验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com