
下列各组离子或分子在溶液中能大量共存,且满足相应要求的是 (. )
| 选项 | 离子或分子 | 要求 |
| A | K+ 、NO3-、Cl-、HS- | c(K+)<c(Cl-) |
| B | Fe3+、NO3-、SO32-、Cl- | 滴加盐酸立即有气体产生 |
| C | NH4+、Al3+、SO42-、CH3COOH | 滴加NaOH溶液立即有气体产生 |
| D | N a+、HCO3-、Mg2+、SO42- | 逐滴滴加氨水立即有沉淀产生 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
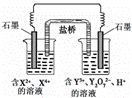 右下图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是
右下图所示原电池工作时,右池中Y2O72-转化为Y3+。下列叙述正确的是
A.左池电极反应式:X4+ + 2e-=X2+
B.每消耗1mol Y2O72-,转移3mol电子
C.改变右池溶液的c(H+),电流强度不变
D.左池中阴离子数目增加
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的分子中既有σ键又有π键的是( )
①HCl ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥C2H2
A.①②③ B.③④⑤⑥ C.①③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。完成下列填空:
(1)Se和浓HNO3反应的还原产物为NO和NO2,且NO和NO2的物质的量之比为1:1,写出Se和浓HNO3的反应方程式
(2)已知:Se+2H2SO4(浓) = 2SO2↑+SeO2+2H2O
2SO2+SeO2+2H2O = Se+2SO42-+4H+
SeO2、H2SO4(浓)、SO2的氧化性由强到弱的顺序是
(3)回收得到的SeO2的含量,可以通过下面的方法测定:
①SeO2+KI+HNO3→Se+I2+KNO3+H2O
②I2+2Na2S2O3 = Na2S4O6+2NaI
配平方程式①,标出电子转移的方向和数目
(4)实验中,准确称量SeO2样品0.1500g,消耗了0.2000 mol/L的Na2S2O3溶液25.00 mL,所测定的样品中SeO2的 质量分数为
质量分数为
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化属于物理变化的是 ( )
A.氧气在放电条件下变成臭氧,
B.胆矾在加热条件下变成白色无水硫酸铜
C.漂白的草帽久置空气中变黄
D.氢氧化铁胶体加入硫酸镁产生沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”, S2O32-与Cl2反应的产物之一为SO42一。下列说法中,错误的是 ( )
A.该反应中的氧化剂是C12
B.SO2与氯水的漂白原理相同,所以可用S02做纺织工业的漂白剂
C.上述反应中,每生成1 mol SO42一,可脱去2 mol C12
D.根据该反应可判断还原性:S2O32->C1—
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生反应:aA(g) 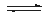 cC(g)+dD(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍。下列叙述正确的是( )
cC(g)+dD(g)反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍。下列叙述正确的是( )
A.A的转化率变大 B.平衡向正反应方向移动
C.D的体积分数变大 D.a<c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
从淡化海水中提取溴的流程如下:
通入Cl2Ⅰ通入空气吹出Br2用X吸收 Ⅱ通入Cl2Ⅲ—Ⅳ→
下列有关说法不正确的是( )
A.X试剂可用Na2SO3饱和溶液
B.步骤Ⅲ的离子反应:2Br-+Cl2=2Cl-+Br2
C.工业上每获得1molBr2,需要消耗Cl244.8L
D.步骤Ⅳ包含萃取、分液和蒸馏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com