
科目:高中化学 来源: 题型:
汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3 = K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断正确的是( )
A.生成40.0LN2(标准状况)
B.有0.250molKNO3被氧化
C.转移电子的物质的量为2.5mol
D.被氧化的N原子的物质的量为3.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子或分子在溶液中能大量共存,且满足相应要求的是 (. )
| 选项 | 离子或分子 | 要求 |
| A | K+ 、NO3-、Cl-、HS- | c(K+)<c(Cl-) |
| B | Fe3+、NO3-、SO32-、Cl- | 滴加盐酸立即有气体产生 |
| C | NH4+、Al3+、SO42-、CH3COOH | 滴加NaOH溶液立即有气体产生 |
| D | N a+、HCO3-、Mg2+、SO42- | 逐滴滴加氨水立即有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于Na202的叙述,正确的是 ( )
A.Na202晶体中的阴离子与阳离子的物质的量之比为1:1
B.Na202晶体为离子晶体,且含极性共价键
C.Na202应保存于密封、干燥带玻璃塞的广口瓶中
D.Na202与盐酸反应,不仅有盐和水生成,同时会放出无色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)向MnSO4和硫酸的混合溶液里加入K2S208(过二硫酸钾),溶液中会发生如下反应:Mn2++ S2082-+H2O→MnO4-+SO42一十H+该反应常用于检验Mn2+的存在。其特征现象是 。
若反应中有0.1 mol还原剂参加反应,则消耗氧化剂的物质的量为 mol。
(2)若该反应所用的硫酸锰改为氯化锰,当它跟过量的过硫酸钾反应时,除有高锰酸钾、硫酸钾、硫酸生成外,其他的生成物还有 。
(3)将NaBiO3固体(黄色微溶)加入到MnSO3和H2S04的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:
NaBi03+ MnSO4+ H2S04→ Na2S04+ Bi2(S04)3+ NaMnO4+ H2O
①配平上述反应的化学方程式;
②上述反应中还原产物是 。
③用单线桥表示该氧化还原反应
(4)S2O82-在一定条件下,可转变为S2O32-,写出往K2S2O3中滴加稀硫酸的离子方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组热化学方程式中,化学反应的△H前者大于后者的是 ( )
①C(s)+O2(g) CO2(g); △H1 C(s)+1/2O2(g)
CO2(g); △H1 C(s)+1/2O2(g)  CO(g); △H2
CO(g); △H2
②S(s)+O2(g)  SO2(g); △H3 S(g)+O2(g)
SO2(g); △H3 S(g)+O2(g)  SO2(g); △H4
SO2(g); △H4
③H2(g)+1/2O2(g) H2O(l); △H5 2H2(g)+O2(g)
H2O(l); △H5 2H2(g)+O2(g)  2H2O(l); △H6
2H2O(l); △H6
④CaCO3(s)  CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)
CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)  Ca(OH)2(s);△H8
Ca(OH)2(s);△H8
A.① B.④ C.②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g)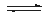 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )

A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C.图Ⅱ表示t0时刻通入氦气对反应速率的影响
D.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的装置中,金属a能从酸中置换出H2,b为碳棒,关于此装置的各种叙述中不正确的是( )
A.碳棒上有气体放出,溶液pH值变大
B.a是正极,b是负极
C.导线中有电子流动,电子从a极到b极
D.a极上发生了氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com