
【题目】据题目要求完成下列各题:
(1)少量的NaHCO3与Ca(OH)2反应的离子反应方程式____________。
(2)用双线桥标出方程式2KMnO4=K2MnO4 + MnO2 + O2中电子转移的方向和数目______________。
(3)用双线桥标出方程式6HCl + KClO3= KCl +3Cl2 +3H2O 中电子转移的方向和数目_______,并指出氧化产物与还原产物的物质的量的比___________。
(4)在MnO2+4HCl=MnCl2+Cl2+2H2O中氧化剂与还原剂的物质的量的比_______,当0.4molHCl被氧化时,则生成标准状况下的Cl2的体积为__________。
【答案】 HCO3-+ Ca2++ OH-=CaCO3↓+H2O 
 5:1 1:2 4.48L
5:1 1:2 4.48L
【解析】(1)少量的NaHCO3与Ca(OH)2反应,按计量数比为1:1比例反应,NaHCO3 + Ca(OH)2 = CaCO3↓+ NaOH + H2O(氢氧化钙过量),离子反应方程式:HCO3- + Ca2+ + OH- =CaCO3↓+ H2O;(2)在反应2KMnO4=K2MnO4 + MnO2 + O2↑中,Mn由+7价分别降为+6价和+4价,氧由-2价升高为0价,共变4价,电子转移的方向和数目是 ;(3)该反应中,氯酸钾中氯元素的化合价由+5价变为0价,所以氯酸钾是氧化剂,HCl中Cl元素化合价由-1价升高到0价,被氧化,氯气既是氧化产物也是还原产物,因得电子与失电子个数相等,氧化产物和还原产物的质量之比是5:1,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子,则电子转移的方向和数目为
;(3)该反应中,氯酸钾中氯元素的化合价由+5价变为0价,所以氯酸钾是氧化剂,HCl中Cl元素化合价由-1价升高到0价,被氧化,氯气既是氧化产物也是还原产物,因得电子与失电子个数相等,氧化产物和还原产物的质量之比是5:1,只有Cl元素化合价发生变化,当有3mol Cl2生成时,转移5mol电子,则电子转移的方向和数目为 ;(4)二氧化锰中Mn元素化合价降低,是氧化剂,HCl中Cl元素化合价升高,是还原剂,同时HCl其酸的作用,各占一半,故氧化剂与还原剂的物质的量之比=1:2;由方程式,当有2molHCl被氧化时,生成标准状况下22.4L,当0.4molHCl被氧化时,则生成标准状况下的Cl2的体积为
;(4)二氧化锰中Mn元素化合价降低,是氧化剂,HCl中Cl元素化合价升高,是还原剂,同时HCl其酸的作用,各占一半,故氧化剂与还原剂的物质的量之比=1:2;由方程式,当有2molHCl被氧化时,生成标准状况下22.4L,当0.4molHCl被氧化时,则生成标准状况下的Cl2的体积为![]() ,V=4.48L。
,V=4.48L。


科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
A.标准状况下,1L庚烷所含有的分子数为 ![]()
B.1mol甲基(﹣CH3)所含电子数为9NA
C.标准状况下,B2H6和C2H4的混合气体22.4L,所含的电子数为16NA
D.26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 将 AgCl 放入水中不能导电,故 AgCl 不是电解质
B. CO2溶于水得到的溶液能导电,所以 CO2 是电解质
C. 金属能导电,所以金属是电解质
D. 固态的 NaCl 不导电,熔融态的 NaCl 能导电,NaCl 是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于(NH4)2SO4溶液,下列说法正确的是( )
A.溶液中存在电离平衡:(NH4)2SO4?2NH ![]() +SO
+SO ![]()
B.向溶液中滴加少量浓硫酸,c(NH ![]() )与c(SO
)与c(SO ![]() )均增大
)均增大
C.加水稀释,溶液中所有离子的浓度均减小
D.溶液中:c(SO ![]() )=2c(NH
)=2c(NH ![]() )+2c(NH3?H2O)
)+2c(NH3?H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1mol·L-1 的FeCl3 溶液逐滴滴入沸水中,液体变为_________色,得到的是Fe(OH)3胶体;反应的化学方程式为_______________________.
用此分散系进行实验:
(1)将其装入U型管内,用石墨棒做电极,接通直流电源,通电一段时间后发现阴极附近颜色____________,这表明___________________,这种现象称为_______________。
(2)向其中加入饱和的(NH4)2SO4溶液,发生的现象是_______________;原因是______________。
(3)向其中逐滴加入过量稀硫酸,现象是__________________;原因是________。
(4)提纯此分散系的方法叫__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下面的反应路线及所给信息填空. 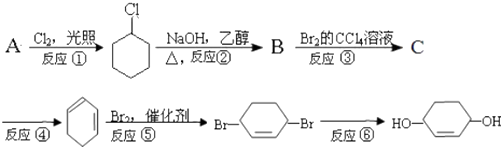
(1)A的结构简式为
(2)在①~⑥的各步反应中,属于取代反应的有 , 属于加成反应的有 .
(3)反应④所用的试剂和条件是 .
(4)反应③的化学方程式是 .
(5)反应⑥的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图,则此有机物可发生的反应类型有( ) ①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和.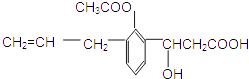
A.①②③⑤⑥
B.②③④⑤⑥
C.①②③④⑤⑥
D.全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在托盘天平的两盘,放上质量相等的A、B两烧杯,调至平衡,然后分别倒入质量相等的足量盐酸,继而在AB两烧杯中放入下述各组物质,结果天平仍保持平衡的是( )
A. 等质量的Na和Mg B. 0.1molZn和0.1molAl
C. 8.4gMgCO3和8.4gNaHCO3 D. 10gCaCO3和10gMgCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在______里或______下能够导电的化合物叫做电解质。电解质溶液之所以能够导电,是由于它们在溶液中发生了______,产生了______。电离时生成的______离子全部是______的化合物叫做酸;生成的______离子全部是______的化合物叫做碱。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com