
����Ŀ��ij��ͬѧ������ʵ��̽��Fe2+��Fe3+�����ʡ��ش��������⣺
(1)�ֱ�ȡһ�����Ȼ������Ȼ��������壬�����Ƴ�0.1mol/L����Һ����FeCl2��Һ�������������м����Ŀ����_____ ___��
(2)����ͬѧȡ2mL FeCl2��Һ�����뼸����ˮ���ټ���1��KSCN��Һ����Һ��죬˵��Cl2�ɽ�Fe2+������FeCl2��Һ����ˮ��Ӧ�����ӷ���ʽΪ_____ __��
(3)����ͬѧ��Ϊ�����ʵ�鲻���Ͻ�������ͬѧ��2mLFeCl2��Һ���ȼ���0.5mLú�ͣ�����Һ�������μ��뼸����ˮ��l��KSCN��Һ����Һ��죬ú�͵�������____ __��
(4)����ͬѧȡ10 mL0.1mol/L KI��Һ������6mL0.1mol/LFeCl3��Һ��ϡ��ֱ�ȡ2mL����Һ��3 ֧�Թ��н�������ʵ�飺
�� ��һ֧�Թ��м���1mLCCl4��������ã�CCl4�����ɫ��
�� �ڶ�ֻ�Թ��м���1��K3Fe(CN)6] ��Һ��������ɫ������
�� ����֧�Թ��м���1��KSCN��Һ����Һ��졣
ʵ���������������_____________(�����ӷ���)��ʵ��������˵������I- ����������£���Һ���Ժ��� ___(�����ӷ���)���ɴ˿���֤����������ԭ��ӦΪ___ ___��
(5)����ͬѧ��ʢ��H2O2��Һ���Թ��м��뼸���ữ��FeCl2��Һ����Һ����ػ�ɫ��������Ӧ�����ӷ���ʽΪ_______ _��һ��ʱ�����Һ�������ݳ��֣������ȣ�����к��ɫ�������ɡ��������ݵ�ԭ����__ ____�����ɳ�����ԭ����____ __(��ƽ���ƶ�ԭ������)��
���𰸡�
(1)��ֹFe2+��������
(2)2Fe2++Cl2=2Fe3++2Cl-��
(3)��������(�ų�������ʵ���Ӱ��)��
(4)Fe2+�� Fe3+�����淴Ӧ��
(5)H2O2+2Fe2++2H+=2Fe3++2H2O��Fe3+��H2O2�ֽ����O2��H2O2�ֽⷴӦ���ȣ��ٽ�Fe3+��ˮ��ƽ�������ƶ���
��������
���������(1)�����Ȼ�����Ӧ�����Ȼ���������FeCl2��Һ�������������м����Ŀ���Ƿ�ֹ�Ȼ��������������ʴ�Ϊ����ֹ�Ȼ�������������
(2)���������������������Ȼ�����Ϊ�Ȼ�������Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+=2Fe3++2Cl-���ʴ�Ϊ��Cl2+2Fe2+=2Fe3++2Cl-��
(3)ú�Ͳ�����ˮ���ܶȱ�ˮС���ֲ����Ը�����Һ������Ӵ����ų�������ʵ���Ӱ�죬�ʴ�Ϊ���������(�ų�������ʵ���Ӱ��)��
(4)����1��K3[Fe(CN)6]��Һ��������ɫ�������������ӵļ���������Ӧ����ʵ���������������Fe2+������һ֧�Թ��м���1mL CCl4��������ã�CCl4������ɫ˵������I2�������ӱ�����������Ϊ�ⵥ�ʣ���Ӧ�����ӷ���ʽΪ��Cl2+2Fe2+=2Fe3++2Cl-��������֧�Թ��м���1��KSCN��Һ����Һ��죬˵����Ũ�ȱ�С����������ϡ���Ȼ�����Һ�в�����������ԭ��Ӧ���Ժ��������ӣ���I-����������£���Һ���Ժ���Fe3+��˵���÷�ӦΪ���淴Ӧ���ʴ�Ϊ��Fe2+��Fe3+�����淴Ӧ��
(5)��ʢ��H2O2��Һ���Թ��м��뼸���ữ��FeCl2��Һ����Һ����ػ�ɫ��˵����������������������Ϊ�����ӣ���Ӧ�����ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O�������ӶԹ�������ֽ��������ã��������ݵ�ԭ��������������������ֽ�����ֽ������������Ȼ�����Һ�д���ˮ��ƽ�⣬Fe3++3H2O![]() Fe(OH)3+3H+��ˮ�ⷴӦΪ���ȷ�Ӧ����������ֽ�ų��������ٽ�Fe3+��ˮ��ƽ�������ƶ����ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O������������������ֽ�����ֽ�������������������ֽⷴӦ���ȣ��ٽ�Fe3+��ˮ��ƽ�������ƶ���
Fe(OH)3+3H+��ˮ�ⷴӦΪ���ȷ�Ӧ����������ֽ�ų��������ٽ�Fe3+��ˮ��ƽ�������ƶ����ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O������������������ֽ�����ֽ�������������������ֽⷴӦ���ȣ��ٽ�Fe3+��ˮ��ƽ�������ƶ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ͬ�ֹ�����Ƭ�ֱ����������ʻ�ϣ�������������������
A. 0.1 mol/L������15mL B. 0.15 mol/L��������Һ8mL
C. 0.4 mol/L������12mL D. 18 mol/L��Ũ����15mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ҫ�ɷֿɱ�ʾΪFeO��Cr2O3��������MgO��Al2O3��Fe2O3�����ʣ��Ը�����Ϊԭ���Ʊ��ظ������K2Cr2O7���Ĺ������������ֲ���������������
���������̼���ƻ���ڿ����г�ֱ��ա�
���պ�Ĺ����ˮ��ȡ������õ���ҺA����A��
������ҺA�м�������pHԼ7��8������õ���ҺB����B��
����������ҺB�м����Ӵ����ữ��ʹ��ҺpHС��5��
������������Һ�м����Ȼ��أ��õ��ظ���ؾ��塣
��1�����б��շ����ķ�Ӧ���£���ƽ����д��ȱ��
�� FeOCr2O3 + Na2CO3 + �� = Na2CrO4 + Fe2O3 + CO2��
�� Na2CO3+Al2O3=2NaAlO2+CO2��
��2������A����Ҫ���� ����д��ѧʽ����
��3�����з�����Ӧ�Ļ�ѧ����ʽ�ǣ�Na2Cr2O7+2KCl=K2Cr2O7��+2NaCl����֪�±�����
���� | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
�ܽ�� ��g/100gˮ�� | 0�� | 28 | 35��7 | 4��7 | 163 |
40�� | 40��1 | 36��4 | 26��3 | 215 | |
80�� | 51��3 | 38 | 73 | 376 | |
���K2Cr2O7����IJ����ɶಽ��ɣ������ǣ�����KCl���塢 �����ˡ�ϴ�ӡ�����õ����塣ϴ�ӳ����IJ���Ϊ ��
��4�����й���B����Ҫ��������������������þ���������ܻ����P���������ʣ���ȷ��������B���������������ķ����ǣ���ȡn g��Ʒ��������� ����д�Լ����������ܽ⡢���ˡ���ͨ�������CO2�����ա���ȴ���������ø������m g��������Ʒ��������������������Ϊ ���ú�m��n�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(Cr)��ҵ��ˮ�Ĵ���ԭ���ǽ�Cr2O72-ת��ΪCr3�����ٽ�Cr3��ת��Ϊ������ת�������У���ˮpH��Cr2O72-ת��ΪCr3���Ĺ�ϵ��ͼ1��ʾ��ʵ����ģ�ҵ��ⷨ����������ˮ��װ����ͼ2��ʾ��

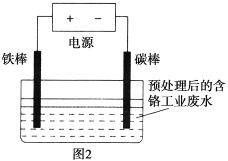
���������֪ʶ�ش��������⣺
(1)������ˮԤ�����ķ�����__________________��
��2��д�����з�Ӧ�����ӷ���ʽ��
���������е�������Ӧʽ___________________________��
��Cr2O72-ת��ΪCr3�������ӷ���ʽ_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ĵ��ѽ�ɰ��������ַ�ʽ���У�C4H10��C2H6+C2H4��C4H10��CH4+C3H6��ij��ѧ��ȤС���ͬѧΪ�ⶨ�����ѽ�����CH4�����ʵ��������ʵ����ͼ��ʾ��

(ע��CuO�ܽ���������CO2��H2O�� Al2O3�Ǵ�����G����װ����ʡ�ԡ�)
��ͼ���Ӻ�װ�ú�����е�ʵ������У�����D��Gװ�ü��ȣ����������װ�õ������ԣ����ž�װ���еĿ�����
��1���������������Ⱥ�˳�������ǣ� ��
��2��Bװ������������� ��
��3��д��C2H6��G�еĻ�ѧ����ʽ�� ��
��4��ʵ�����ж�Eװ���еĻ���ﰴ��ͼ������
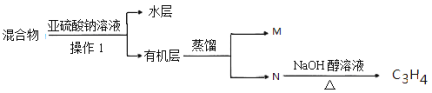
������I���õ����������� ��д��M�ķ���ʽ ��
������������Һ��������(�����ӷ���ʽ��ʾ) ��
��5���ٶ�������ȫ�ѽ⣬������װ���е���������ȫ��Ӧ����(E��F)װ�õ��������ȷ�Ӧǰ������15.4g��Gװ���й�������������30.4g��������ѽ������n(CH4)= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ����������ʵ������Ԥ����ȷ����

A. ʵ��������εμ�����ʱ���Թ�������������������
B. ʵ������������ã��²���ҺΪ�Ⱥ�ɫ���ϲ���ɫ
C. ʵ�������ӱ���ʳ��ˮ����ȡNaCl����
D. װ����������KMnO4��Һ�������ݳ��֣�����Һ��ɫ����dzֱ����ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ϩ�����Ȼ�̼�����ķ�����
A. ���Ը������ B. ˮ C. Һ�� D. ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݡ��ݴ�����˵���������
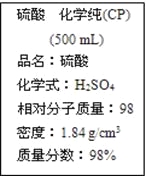
A. ����������ʵ���Ũ��Ϊ18.4 mol/L
B. �����᳣���������
C. ����200 mL 4.6 mol/L��ϡ������ȡ������50 mL
D. ���������������ˮ��Ϻ�������Һ��Ũ�ȴ���9.2 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
��̼Ԫ�ز��������������л���������
�������ϵ���������̼Ԫ�صĻ����Ͻ���������
��̼Ԫ���Ǹ��ִ���ӻ���������������Ԫ��
��̼Ԫ����������������л�������������Ԫ��
A. �ڢۢ� B. �ۢ� C. �ڢ� D. �٢ۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com