
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图所示:

(1)从反应开始到10 s时,用Z表示的反应速率为 ,X的物质的量浓度减少了 ,Y的转化率为 。
(2)该反应的化学方程式为
(3)10 s后的某一时刻(t1)改变了外界条件,其速率随时间的变化图像如图所示:

则下列说法符合该图像的是 。
A.t1时刻,增大了X的浓度 B.t1时刻,升高了体系温度
C.t1时刻,缩小了容器体积 D.t1时刻,使用了催化剂
【答案】(1)0.079 mol·L-1·s-1 0.395 mol·L-1 79.0%
(2)X(g)+Y(g)![]() 2Z(g)
2Z(g)
(3)CD
【解析】(1)分析图像知:
v(Z)= ![]() =0.079 mol·L-1·s-1,
=0.079 mol·L-1·s-1,
Δc(X)= ![]() =0.395 mol·L-1,
=0.395 mol·L-1,
Y的转化率α(Y)=![]() ×100%=79%。
×100%=79%。
(2)由各物质转化的量:X为0.79 mol,Y为0.79 mol,Z为1.58 mol可知方程式中各物质的化学计量数之比为1∶1∶2,则化学方程式为X(g)+Y(g)![]() 2Z(g)。
2Z(g)。
(3)由图像可知,外界条件同等程度地增大了该反应的正、逆反应速率。增大X的浓度、升高体系温度均不会同等程度地改变正、逆反应速率,A、B错误。该反应为反应前后气体体积不变的反应,缩小容器体积或增大压强,均可同等程度地增大正、逆反应速率,C正确。D使用催化剂可同等程度地改变正、逆反应速率,D正确。


科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F是元素周期表中前36号元素,它们的原子序数依次增大。A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E4+与氩原子的核外电子排布相同。F是第四周期d区原子序数最大的元素。请回答下列问题:
(1)写出E的价层电子排布式 。
(2)A、B、C、D电负性由大到小的顺序为________________(填元素符号)。
(3)F(BD)4为无色挥发性剧毒液体,熔点-25℃ ,沸点43℃。不溶于水,易溶于乙醇、乙醚、苯等有机溶剂,呈四面体构型,该晶体的类型为 ,F与BD之间的作用力为 。
(4)开发新型储氢材料是氢能利用的重要研究方向。
①由A、B、E三种元素构成的某种新型储氢材料的理论结构模型如图1所示,图中虚线框内B原子的杂化轨道类型有 种;
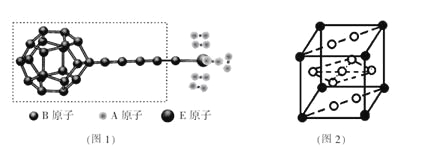
②分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料。X一定不是 (填标号);
A.H20 B. CH4C.HF D.CO(NH2)2
③F元素与镧( La)元素的合金可做储氢材料,该晶体的晶胞如图2所示,晶胞中心有一个F原子,其他F原子都在晶胞面上,则该晶体的化学式为 ;已知其摩尔质量为Mg.mol-1,晶胞参数为apm,用NA表示阿伏伽德罗常数,则该晶胞的密度为 g.cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 化学反应除了生成新的物质外,还伴随着能量的变化
B. 据能量守恒定律,反应物的总能量一定等于生成物的总能量
C. 放热反应不需要加热就能发生
D. 吸热反应不加热就不会发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应AsO43-+2I-+2H+![]() AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
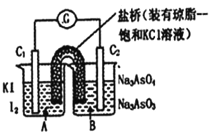
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现电流计指针均发生偏转.据此,下列判断正确的是
A.Ⅰ操作过程中,C2棒上发生的反应为:AsO43-+2H++2e-=AsO33-+H2O
B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液
C.操作Ⅰ过程中,C1为正极
D.Ⅱ操作过程中,C1棒上发生的反应为:2I-_2e-=I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.15mol的MnO2与过量的12mol/L的浓盐酸反应,与50mL12mol/L的浓盐酸与过量MnO2反应,两者产生的氯气相比(其它反应条件相同)( )
A.一样多
B.后者较前者多
C.前者较后者多
D.无法比较
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下仪器,仪器中已注入溶液,回答下列问题。
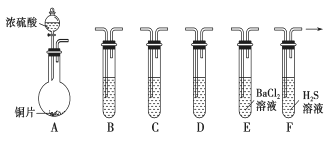
(1)加热装置A,写出铜与浓硫酸反应的化学方程式:_______________________________
(2)验证碳、硅非金属性的相对强弱(已知酸性:H2SO3>H2CO3),若选择仪器A、B、C、D并相连接,则B、C、D中所选择的试剂为B________、C________、D________。能说明碳的非金属性比硅强的实验现象是_________________。
(3)验证SO2的氧化性、还原性。若选择A、E、F仪器,并按A、E、F顺序连接。
①则证明SO2有氧化性的实验现象是________________,反应方程式为________________。
②若证明SO2具有还原性,在E中采取的实验操作为_________________________________,
其实验现象为__________________,反应原理为__________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是( )
A. 第一块钠失去电子多 B. 两块钠的反应产物质量一样大
C. 第二块钠的反应产物质量大 D. 两块钠失去电子一样多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备硫酸常用接触法,工业上制硝酸常用氨的催化氧化法。下列关于工业上制硫酸与硝酸的说法中不正确的是( )
A. 在沸腾炉中进行的反应为:4FeS2+11O2![]() 2Fe2O3+8SO2
2Fe2O3+8SO2
B. 工业上制硫酸与硝酸都用到同一工艺设备:吸收塔
C. 硫酸工业、硝酸工业都需要对工业尾气进行处理
D. 工业上制备硫酸和制硝酸涉及的反应都属于氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com