
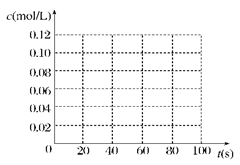
(13��)��100��ʱ����0.100 mol ������������������� 1 L ������յ��ܱ������У���һ��ʱ��Ը������ڵ�����Ũ�Ƚ��з����õ��±����ݣ�
| ʱ��(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)(mol/L) | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)(mol/L) | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ������ʡ�����и�����ѧ������⣨�������ۻ�ѧ�Ծ��������棩 ���ͣ������
�л���G������ʽΪ C13H18O2����һ�����ϣ���ϳ�·������ͼ��ʾ������A��һ����Է�������Ϊ70�������˴Ź����������ĸ����ҷ����֮��Ϊ6:2:1:1��B��һ�ַ����庬���������Է���������100-130֮�䣬B�к���Ԫ�ص���������Ϊ13��1%��F����ʹ������Ȼ�̼��Һ��ɫ��
��֪��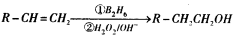
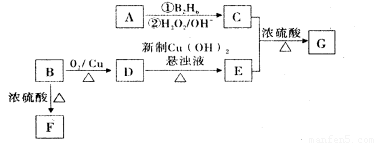
��ش���������⣺
��1��������A�Ľṹ��ʽΪ____����ϵͳ������������������____��
��2��������B�ķ���ʽΪ____��B����ͼת���з����ķ�Ӧ�����ķ�Ӧ������____��
��3��д��D��E��Ӧ�Ļ�ѧ����ʽ____��
��4��д��C��E����G��Ӧ�Ļ�ѧ����ʽ____��
��5��E��ͬ���칹���ж��֣�д�����������������������ʵĽṹ��ʽ____��
a�����ڷ����廯�����ұ����ϵ�һ�ȴ��������֣�b�����С�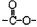 ������
������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014������ʡ��һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
(13��)��100��ʱ����0.100 mol ������������������� 1 L ������յ��ܱ������У���һ��ʱ��Ը������ڵ�����Ũ�Ƚ��з����õ��±����ݣ�
|
ʱ��(s) |
0 |
20 |
40 |
60 |
80 |
|
c(N2O4)(mol/L) |
0.100 |
c1 |
0.050 |
c3 |
c4 |
|
c(NO2)(mol/L) |
0.000 |
0.060 |
c2 |
0.120 |
0.120 |
(1)�÷�Ӧ��ƽ�ⳣ������ʽΪ______________________��
�ӱ��з�����c1________c2��c3________c4(�>������<������)��
(2)����ͼ�л����������˷�Ӧ��c(N2O4)��c(NO2)��Ũ����ʱ��仯�����ߡ�

(3)�����������£��ӷ�Ӧ��ʼֱ���ﵽ��ѧƽ��ʱ��������������ƽ����Ӧ����Ϊ__ mol/(L��s)��
(4)��Ӧ�ﵽƽ���,���������ĸı��ʹNO2�����Ũ���������
A�������������ݻ������� B���ٳ���һ������N2O4
C�������һ������NO2 D���ٳ���һ������He
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����Ӧԭ����C2H5OH+NaBr+H2SO4![]() NaHSO4+C2H5Br+H2O
NaHSO4+C2H5Br+H2O
(2)��Ҫװ�ü���ͼ
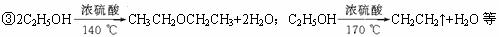
��3����������
����100 mLԲ����ƿ�м���10 mL 95%�Ҵ���28 mL 78%���ᣬȻ�������ϸ��13 g�廯�ơ��ڼ��뼸�����Ƭ��С��ҡ����ƿʹ����ȡ�����ƿ��ֱ���������������������¶����ӽ���������С�ļ��ȣ�ʹ���ַ�Ӧ���ٽ�������ֱ��������������Ϊֹ�����ٽ���ƿ��Һ����ȴ��������������Һ��ϴ�ӷ�Һ��
�Իش��������⣺
�ٱ�ʵ���õ���78%�����ᣬΪ�β���Ũ���________________________________��
������������Һ��������____________________________________________________��
�۸�ʵ���л�������������л���ĸ���Ӧ��д����ѧ����ʽ��________________________________����һ������
�ܱ���ʵ��ֻ�ռ���5 mL�����飬���������Լ10 mL�٣�ԭ�����������ӷ���Ե�ʣ�Ϊ�˼�������ʧ������Ϊ�ɲ�ȡʲô��ʩ��________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
(��8��)(1)��ij�¶��£�H2O�����ӻ�����Ϊ1��10-13�����ڸ��¶���
��0.01mol/LNaOH��Һ��pH= ��
��100mL 0.1mol/L H2SO4��Һ��100mL 0.4mol/L��KOH��Һ��Ϻ�pH=
��2��pHֵ��ͬ�� ��HCl��aq���� ��H2SO4��aq���� �� CH3COOH��aq����100 mL
��������Һ�����ʵ���Ũ�������� ��
�ڷֱ���0.1 mol/L��NaOH��aq���кͣ���������NaOH��aq�������� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com