
| A. | 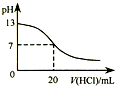 如图表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0.1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 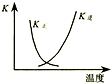 图中曲线表示反应2SO2(g)+O2(g)?2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 | |
| C. | 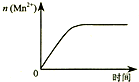 图③表示10 mL 0.01 mol•L-1 KMnO4 酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. | 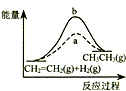 图中a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
分析 A、当溶液pH=7时,氢氧化钠就与氯化氢恰好反应,滴定曲线应该有一个滴定突变;
B、该反应为放热反应,温度升高,平衡向着逆向移动,K(逆)增大、K(正)减小;
C、高锰酸钾和草酸之间反应生成锰离子、二氧化碳和水;
D、反应物的能量低于产物能量,反应是吸热的,加入催化剂可以降低反应的活化能,但是不会改变反应的焓变.
解答 解:A、用盐酸滴定氢氧化钠溶液,当恰好中和时溶液的pH=7,酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,题中图象变化与实际不相符,故A错误;
B、因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K(逆)会增大,而K(正)会减小,图象中变化与实际上的变化相符,故B正确;
C、KMnO4 酸性溶液与过量的H2C2O4溶液混合时,反应生成锰离子、二氧化碳和水,n(Mn2+) 随时间的延长而增加,直到不再变化,故C正确;
D、反应物的能量低于产物能量,反应是吸热的,焓变是正值,加入催化剂可以降低反应的活化能,但是不会改变反应的焓变,故D错误.
故选BC.
点评 题以图象与中和滴定、化学平衡、反应热的确定等知识,题目难度中等,注意抓住图象的“形变神不变”对图象进行分析,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:填空题
 现有A、B、C三种烃,其球棍模型如图:
现有A、B、C三种烃,其球棍模型如图:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na>Be>C>F | B. | S2->S>O>F | C. | S2->Cl->K+>Ca2+ | D. | Cl>Li>N>He |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁的金属活泼性强,故不能用钢瓶来盛放液氯 | |
| B. | Na2O2与CO2能反应产生氧气,用作呼吸面具和潜水艇供氧剂 | |
| C. | NaHCO3受热能分解产生CO2气体,在食品工业中可作为焙制糕点的膨松剂 | |
| D. | 常温下浓硫酸能使铝发生钝化,常温下可用铝制容器贮藏贮运浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) | |
| B. | 混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) | |
| C. | 加入AgNO3溶液时首先生成AgCl沉淀 | |
| D. | 混合溶液中$\frac{c(C{l}^{-})}{c({I}^{-})}$的值约为1.02×10-6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol的氨气与1mol的铵根离子所含电子数、质子数均为10NA | |
| B. | 14g乙烯和14g聚乙烯所含的原子数均为3NA | |
| C. | 标准状况下,11.2LCH3CH20H中含有的C-H键的个数为2.5NA | |
| D. | 1L1mol•L-1的NaAl02溶液中含有Al02-的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种物质所含原子个数之比为4:3 | |
| B. | 两种物质与水充分反应,生成的氢氧化钠质量之比为2:1 | |
| C. | 两种物质与足量的CO2反应,消耗气体的质量比为1:1 | |
| D. | 两种物质中阳离子的物质的量之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
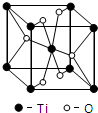 第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.
第四周期过渡元素Mn、Fe、Ti可与C、H、O形成多种化合物.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com