下列叙述正确的是( )
A.若R2-和M+的电子层结构相同.则离子半径R2-<M+
B.标准状况下,11.2 L氮气和氧气的混合气所舍原子数约为6.02×1023
C.PH3和HCI各原子最外层均满足8电子结构,且都是含有18个电子的分子
D.将AgCl和AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,只有AgBr沉淀的生成
【答案】
分析:A、R
2-和M
+的电子层结构相同,核电荷数M大于R,电子层结构相同核电荷数越大离子比较越小.
B、标准状况下,11.2 L氮气和氧气的物质的量为0.5mol,氮气与氧气都是双原子分子,所以原子的物质的量为1mol,再根据N=nNA计算.
C、分子中H原子不满足8电子结构.
D、AgCl和AgBr的饱和溶液等体积混合,再加入足量浓AgNO
3溶液,会生成AgCl、AgBr沉淀.
解答:解:A、R
2-和M
+的电子层结构相同,核电荷数M大于R,电子层结构相同核电荷数越大离子比较越小,所以离子半径
R
2->M
+,故A错误;
B、标准状况下,11.2 L氮气和氧气的物质的量为
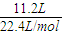
=0.5mol,氮气与氧气都是双原子分子,所以原子的物质的量为1mol,所含原子数约为6.02×10
23,故B正确;
C、PH
3和HCI都是含有18个电子的分子,P、Cl原子最外层均满足8电子结构,H原子不满足8电子结构,故C错误;
D、AgCl和AgBr的饱和溶液等体积混合,再加入足量浓AgNO
3溶液,银离子浓度增大,会生成AgCl、AgBr沉淀,故D错误.
故选:B.
点评:考查离子半径比较、溶解平衡、分子结构、常用化学计量计算等,难度中等,注意C选项中共价化合物中元素化合价绝对值+原子最外层电子数=8满足8电子结构,分子中含有H原子一定不满足8电子结构.

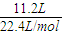 =0.5mol,氮气与氧气都是双原子分子,所以原子的物质的量为1mol,所含原子数约为6.02×1023,故B正确;
=0.5mol,氮气与氧气都是双原子分子,所以原子的物质的量为1mol,所含原子数约为6.02×1023,故B正确;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案