
����Ŀ��������(��Ҫ�ɷ�ΪAl2O3��������SiO2��Fe2O3)�ǹ�ҵ���Ʊ�����������Ҫԭ�ϣ���ҵ����ȡ�������Ĺ����������£�

(1)����A�ijɷ��ǣ��ѧʽ��_________��
(2) ������м������NaOH��Һ������Ӧ�����ӷ���ʽ������H++OH��=H2O������
_____________________________��________________________________��
(3) �������ͨ�����CO2�������������������������___________________��
(4) ȷ��ȡ8g��������Ʒ������һ�����Լ�a����Һ��ʹ���е�Al2O3��Fe2O3ǡ���ܽ���Ȼ��������Һ�м���10mol��L��1��NaOH��Һ���������������������NaOH��Һ�������ϵ��ͼ��ʾ������Ʒ��Al2O3�İٷֺ���Ϊ_________��
���𰸡� SiO2 Fe3++3OH��=Fe(OH)3 Al3++4OH��=[Al(OH)4]�� ����������ʹ���ɵ�Al(OH)3�ܽ� 63.75%
���������������м�������Լ�a��Ȼ�����I�õ�����A����Һ�ף������IΪ���ˣ���Һ���м������NaOH��Һ����II��õ�����B����Һ�ң�����II�ǹ��ˣ�Al2O3��SiO2������ǿ����Һ��Fe2O3������ǿ����Һ��SiO2������ϡ�����Fe2O3��Al2O3������ϡ���ᣬ����ͼ֪����Һ���к�����Ԫ�أ����Լ�aΪϡ���ᣬ����AΪSiO2����Һ��������Ϊ�Ȼ������Ȼ�����HCl������BΪFe(OH)3����Һ���к���NaAlO2��NaOH��NaCl������Һ����ͨ����˶�����̼�õ���Һ̼��������Һ������CΪAl(OH)3���������������õ���������
(1)ͨ�����Ϸ���֪������A SiO2���ʴ�Ϊ��SiO2 ��
(2)������м������NaOH��Һ��ϡ���ᡢ�����ӡ������Ӷ���NaOH��Һ��Ӧ��������Ӧ�����ӷ���ʽ��H++OH-=H2O��Fe3++3OH-=Fe(OH)3����Al3++4OH-=[Al(OH)4]-���ʴ�Ϊ��Fe3++3OH-=Fe(OH)3����Al3++4OH-=[Al(OH)4]-��
(3)�������ͨ�����CO2������������������������ǹ�����ϡ�������ܽ����ɵ������������ò��������������ʴ�Ϊ������������ʹ���ɵ�Al(OH)3�ܽ⣻
(4)����ͼ֪��35-45mLNaOH��Һ���ܽ�Al(OH)3���ܽ�Al(OH)3����NaOH���������Al(OH)3����NaOH��Һ�����![]() ����������Al(OH)3����NaOH��Һ���Ϊ30mL��35mLNaOH��Һʱ�����ӡ���������ȫ����������������������������NaOH��Һ���Ϊ5mL��
����������Al(OH)3����NaOH��Һ���Ϊ30mL��35mLNaOH��Һʱ�����ӡ���������ȫ����������������������������NaOH��Һ���Ϊ5mL��
���ݹ�ϵʽAl2O3��2Al(OH)3��6NaOH֪��n(Al2O3)= ![]() =0.05mol��m(Al2O3)=0.05mol��102g/mol=5.1g����������������=
=0.05mol��m(Al2O3)=0.05mol��102g/mol=5.1g����������������=![]() ��100%=63.75%���ʴ�Ϊ��63.75%��
��100%=63.75%���ʴ�Ϊ��63.75%��


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[2015���]�����йء���ѧ���������������ȷ����
A����ȼ���������ȼ������SO3
B���й��Ŵ�����������Һ���������ͭ�������ͭ��
C�����ð�˾ƥ�ֳ���ˮ���ᷴӦʱ����NaHCO3��Һ�ⶾ
D��ʹ�ú�������Ũ�Ƚϴ�ĵ���ˮϴ�·�������ȥ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CO2ת��Ϊ�״���ԭ��ΪCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H <0��500 ��ʱ�������Ϊ1 L �Ĺ̶��ݻ����ܱ������г���1mol CO2��3mol H2�����CO2Ũ����CH3OH Ũ����ʱ��ı仯��ͼ��ʾ�����еó��Ľ�����������( )
CH3OH(g)+H2O(g) ��H <0��500 ��ʱ�������Ϊ1 L �Ĺ̶��ݻ����ܱ������г���1mol CO2��3mol H2�����CO2Ũ����CH3OH Ũ����ʱ��ı仯��ͼ��ʾ�����еó��Ľ�����������( )

A������X���Ա�ʾCH3OH(g)��H2O(g)��Ũ�ȱ仯
B���ӷ�Ӧ��ʼ��10minʱ��H2�ķ�Ӧ������(H2)=0.225 mol/(L��min)
C��ƽ��ʱH2 ��ת����Ϊ75%
D��500 ��ʱ�÷�Ӧ��ƽ�ⳣ��K=3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����һ������A��B��C�������ʣ��������壩����̶����Ϊ10 L���ܱ������У�һ�������·�����Ӧ��һ��ʱ���ڲ�ø����ʵ����ʵ����仯����ͼ��ʾ��
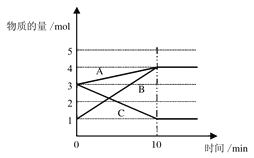
�����������⣺
�ٸ÷�Ӧ�ĵķ�Ӧ����_______������ĸ������������________������ĸ������Ӧ�Ļ�ѧ����ʽ��A��B��C�ɱ�ʾΪ____________________________������ĸ��ʾ��
����B��Ũ�ȱ仯��ʾ��0~10 min�ڵķ�Ӧ������__________
���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�ı�־��___________������ĸ��
a��A��BŨ����� b��A�ٷֺ������ֲ���
c��A������������B������������� d�������������ѹǿ����
e�������л��������ܶȱ��ֲ���
��2����ͭ��п��ϡ������ɵ�ԭ����У�������_______���ѧʽ��������_______��Ӧ���缫��Ӧ��________________________��������_______���ѧʽ��������________��Ӧ���ܵķ�Ӧʽ(���ӷ���ʽ)��______________________��
��3���������ĽǶȿ����Ͽ���ѧ��Ҫ______�����������ջ�ų�����ͬ�����γɻ�ѧ��Ҫ_____����������Ӧ�������������������ʱ���÷�ӦΪ_______��Ӧ�������Ȼ���ȣ���ͬ��������Ӧ�������������������ʱ���÷�ӦΪ__________��Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǿ������Һ���ܴ����������ɫ������������ ��
A��K+��Na+��NO3����MnO4�� B��K+��Na+��Cl����SO42��
C��K+��Na+��Br����Cu2+ D��Na+��Ba2+��OH����SO42��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��C(s)��O2(g)��CO2(g) ��H1
CO2(g)��C(s)��2CO(g) ��H2
2CO(g)��O2(g)��2CO2(g) ��H3
4Fe(s)��3O2(g)��2Fe2O3(s) ��H4
3 CO(g)��Fe2O3(s)��3CO2(g)��2Fe(s) ��H5
���й���������Ӧ�ʱ���ж���ȷ����
A����H1��0����H3��0 B����H2��0����H4��0
C����H1����H2����H3 D����H3����H4����H5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E���ֶ�����Ԫ�ص�ԭ��������������A��C��B��Eͬ���壬C��D��Eͬ���ڡ���A��B��ɵ����ֻ�������Ҷ�ΪҺ̬������A��Bԭ����֮��Ϊ2��1������Ϊ1��1����B��C��ɵ����ֻ�������Ͷ���Ϊ��̬������C��Bԭ����֮��Ϊ2��1������Ϊ1��1��C��D��E������������Ӧ��ˮ��������֮����ܷ�����Ӧ���Ҿ��м����ɣ���AΪԭ�Ӱ뾶��С�Ķ�����Ԫ�أ���Ϊ����ɫ���塣��
��1��D��ԭ�ӽṹʾ��ͼΪ��__________________
��2��AԪ�صĵ���Ϊ��_____________���ѧʽ�������ĵ���ʽΪ��_____________
��3��E�����ڱ��е�λ��_________________________________
��4��C��D������������Ӧˮ�������Ӧ�����ӷ���ʽΪ��
____________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ��2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)��Ƶ�ԭ�����ͼ��ʾ����ش��������⣺
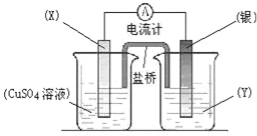
��1���缫X�IJ����� (��ѧʽ)���������ҺY�� ��
��2�����缫Ϊ��ص� ���������ĵ缫��ӦΪ ��X�缫�Ϸ����ĵ缫��ӦΪ ��
��3�����·�еĵ����Ǵ� �缫���� �缫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǿ���Ե���ɫ��Һ���ܴ������������������ ��
A��NH4+��Mg2+��SO42����Cl�� B��Ba2+��K+��OH����NO3��
C��Al3+��Cu2+��SO42����Cl�� D��Na+��Ca2+��Cl����HCO3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com