
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源:不详 题型:填空题
| 元素性质[ | 元素编号 | |||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 原子半径/nm | 0.102 | 0.110 | 0.074 | 0.075 | 0.071 | 0.099 |
| 最高化合价 | +6 | +5 | | +5 | | +7 |
| 最低化合价 | -2 | -3 | -2 | -3 | -1 | -1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.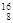 O 与 O 与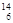 C互为同位素 C互为同位素 | B.加碘食盐能使淀粉溶液变蓝 |
| C.I和Cl是同族元素,HCl比HI稳定 | D.从海带中提取I2的过程只发生物理变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 |
| B.原子最外层电子数为2的元素一定处于周期表IIA族 |
| C.离子化合物中可能含有共价键,但共价化合物中一定不含离子键 |
| D.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有①②正确 | B.只有③④正确 |
| C.全都不正确 | D.全都正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com