
已知断裂1 mol共价键所需要吸收的能量分别为H—H:436 kJ,I—I:151 kJ,H—I:299 kJ,下列对H2(g)+I2(g) 2HI(g)的反应类型判断错误的是( )
2HI(g)的反应类型判断错误的是( )
A.放出能量的反应 B.吸收能量的反应
C.氧化还原反应 D.化合反应
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
实验是研究化学的基础,试回答以下问题:
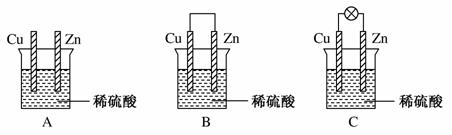
(1)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察锌片上有气泡,再平行插入一块铜片(见图A),可观察到铜片________(填“有”或“没有”)气泡产生。再用导线把锌片和铜片连接起来(见图B),组成一个原电池,负极为________,正极的电极反应式为________;
(2)如果烧杯中最初装入的是500 mL 2 mol·L-1的稀硫酸溶液,构成铜锌原电池(见图C,假设产生的气体没有损失),当在标准状况下收集到11.2 L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=________mol·L-1,c(ZnSO4)=________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物在氧气中充分燃烧,生成等物质的量的二氧化碳和水.则该有机物的组成必须满足的条件是()
A. 分子中C、H、O的个数比为1:2:3
B. 分子中C、H的个数比为1:2
C. 该有机物的相对分子质量为14
D. 该分子中肯定不含氧
查看答案和解析>>
科目:高中化学 来源: 题型:
某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol.试回答:
(1)烃A的分子式为C6H12.
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则燃烧时消耗标准状况下的氧气100.8L.
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为或.
(4)若烃A能使溴水褪色,在催化剂作用下,与氢气加成,其加成产物经测定分子中含有4个甲基.烃A可能有的结构简式为、、.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述或表示方法正确的是( )
A.伴有能量变化的物质变化都是化学变化
B.0.5 mol H2完全燃烧生成水蒸气放出热量121 kJ,H2燃烧的热化学方程式表示为:2H2(g)+O2(g)===2H2O(g) ΔH=-242 kJ·mol-1
C.由C(金刚石)===C(石墨) ΔH=-1.90 kJ·mol-1,可知石墨比金刚石稳定
D.一个化学反应中,当生成物能量大于反应物能量时,反应放热,ΔH为“-”
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组热化学方程式中,化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)===CO2(g) ΔH1
C(s)+ O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3
S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+ O2(g)===H2O(l) ΔH5
O2(g)===H2O(l) ΔH5
2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7
CaO(s)+H2O(l)===Ca(OH)2(s) ΔH8
A.① B.④
C.②③④ D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化过程,属于放热反应的是( )
①液态水变成水蒸气
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥弱酸电离.
|
| A. | ②③④⑤ | B. | ②③④ | C. | ②⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:①101kPa时,C(s)+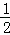 O2(g)=CO(g);△H1=﹣110.5kJ/mol②稀溶液中,H+(aq)+OH﹣(aq)=H2O(1);△H2=﹣57.3kJ/mol,下列结论正确的是( )
O2(g)=CO(g);△H1=﹣110.5kJ/mol②稀溶液中,H+(aq)+OH﹣(aq)=H2O(1);△H2=﹣57.3kJ/mol,下列结论正确的是( )
|
| A. | 若碳的燃烧热用△H3来表示,则△H3<△H1 |
|
| B. | 若碳的燃烧热用△H3来表示,则△H3>△H1 |
|
| C. | 稀硫酸与稀NaOH溶液反应的中和热△H=﹣57.3kJ/mol |
|
| D. | 浓硫酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量 |
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末考试化学试卷(解析版) 题型:填空题
(10分)物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识回答:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为________。
(2)B为0.1 mol·L-1NaHCO3溶液,实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因:________________________________________。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入________,目的是_______________;
若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com