
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 22.4LCl2溶于足量水,所得溶液中Cl2、Cl-、HClO和ClO-四种微粒总数为NA
B. 标准状况下,38g3H2O2中含有3NA共价键
C. 常温下,将5.6g铁块投入足量浓硝酸中,转移0.3NA电子
D. 0.1molL-1MgCl2溶液中含有的Mg2+数目一定小于0.1NA
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
【题目】已知砒霜(As2O3)与锌可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O。
(1)请用“双线桥法”标出电子转移的方向和数目:____________。
(2)砒霜在上述反应中显示出来的性质是_______(填字母)。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化产物是___,还原产物是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.10 mol/L CuCl2溶液中滴加0.10mol/L Na2S溶液,滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示。下列说法正确的是

A. Ksp(CuS)的数量级为10-21
B. 曲线上a点溶液中,c(S2-)c(Cu2+) > Ksp(CuS)
C. a、b、c三点溶液中,n(H+)和n(OH-)的积最小的为b点
D. c点溶液中:c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)![]() 2NO(g) ΔH>0。已知该反应在2 404 ℃时,平衡常数K=64×10-4。请回答:
2NO(g) ΔH>0。已知该反应在2 404 ℃时,平衡常数K=64×10-4。请回答:
(1)某温度下,向2 L的密闭容器中充入N2和O2各1 mol,5分钟后O2的物质的量为0.5 mol,则N2的反应速率为___。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志___(填字母序号)。
A.消耗1 mol N2同时生成1 mol O2
B.混合气体密度不变
C.混合气体平均相对分子质量不变
D.2v正(N2)=v逆(NO)
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是__(填字母序号)。

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气体中NO的体积分数_____(填“变大”“变小”或“不变”)。
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1 mol·L-1、4.0×10-2 mol·L-1和3.0×10-3 mol·L-1,此时反应________________(填“处于化学平衡状态”“向正反应方向进行”或“向逆反应方向进行”),理由是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用硼镁矿(Mg2B2O5·H2O,含Fe2O3杂质)制取硼酸(H3BO3)晶体的流程如下。
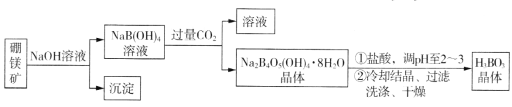
同答下列问题:
(1)沉淀的主要成分为____________________(填化学式)。
(2)写出生成Na2B4O5(OH)4·8H2O的化学方程式_________________________________。
(3)检验H3BO3晶体洗涤干净的操作是______________________________。
(4)已知:
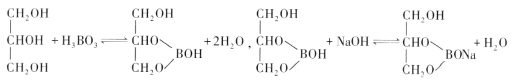
实验室利用此原理测定硼酸样品中硼酸的质量分数。准确称取0.3000g样品于锥形瓶中,加入过量甘油加热使其充分溶解并冷却,滴入1~2滴酚酞试液,然后用0.2000mol·L-1NaOH标准溶液滴定至终点,消耗NaOH溶液22.00mL。
①滴定终点的现象为________________________。
②该硼酸样品的纯度为_________________%(保留1位小数)。
(5)电解NaB(OH)4溶液制备H3BO3的工作原理如下图。
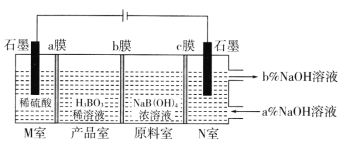
①b膜为________交换膜(填“阴离子”或“阳离子”)。理论上每生成1molH3BO3,两极室共生成__________L气体(标准状况)。
②N室中,进口和出口NaOH溶液的浓度:a%_________b%(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,一定条件下进行反应:mA(气)+nB (气)![]() pC(气)+qD(气),若增大压强,或升高温度,重新达到平衡,
pC(气)+qD(气),若增大压强,或升高温度,重新达到平衡,![]() 随时间化过程均如图所示,则对该反应叙述正确的是
随时间化过程均如图所示,则对该反应叙述正确的是

A. 正反应是放热反应, m+n<p+q
B. 逆反应是放热反应, m+n﹥p+q
C. 正反应是放热反应, m+n﹥p+q
D. 逆反应是放热反应, m+n﹥p+q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(原创)下列说法不正确的是( )
A.中和热测定实验中,应迅速将NaOH溶液和盐酸在测定装置中混合
B.为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可
C.探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL 5%H2O2和1mL H2O,向另一支试管中加入2mL 5%H2O2和1mL FeCl3溶液,观察并比较实验现象
D.已知![]() ,为了利用该反应探究反应速率与温度的关系,所用试剂除1 mol·L-1KI溶液、0.1 mol·L-1稀硫酸外,还需要用到淀粉溶液
,为了利用该反应探究反应速率与温度的关系,所用试剂除1 mol·L-1KI溶液、0.1 mol·L-1稀硫酸外,还需要用到淀粉溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲苯是有机合成的重要原料,既可用来合成抗流感病毒活性药物的中间体E,也可用来合成γ-分泌调节剂的药物中间体K,合成路线如下:

已知:ⅰ.R1NH2+Br-R2![]() R1-NH-R2+HBr
R1-NH-R2+HBr
ⅱ.![]()
(1)A的结构简式为______________。
(2)C中含氧官能团名称为_____________。
(3)C→D的化学方程式为_____________。
(4)F→G的反应条件为________________。
(5)H→I的化学方程式为________________。
(6)J的结构简式为_____________。
(7)利用题目所给信息,以![]() 和
和 为原料合成化合物L的流程如下,写出中间产物1和中间产物2的结构简式:______,_________。
为原料合成化合物L的流程如下,写出中间产物1和中间产物2的结构简式:______,_________。
①
②合成L的过程中还可能得到一种高分子化合物,其结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出下列反应方程式(请注明反应条件),并按要求填空
(1)实验室制备乙烯_______________,反应类型是___________.
(2)乙酸与乙醇的反应______________,反应的无机产物中氧元素的来源是________。
(3)溴乙烷与氢氧化钠水溶液共热_____________,此反应将卤代烃类物质转化为______类物质.
(4)苯与浓硫酸、浓硝酸的混合酸在加热时发生反应__________,反应类型是___________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com