
����Ŀ����֪ij���������к���NaCl���ʣ�Ϊ�ⶨ�����еĴ��������������������ͼ�е�װ�ý���ʵ�顣
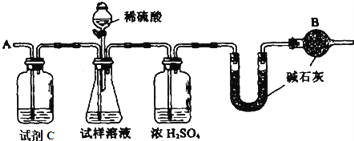
��Ҫʵ�鲽�����£�
�ٰ�ͼ��װ�����������װ�õ�������
�ڽ�a g����������ƿ�У�����������ˮ�ܽ⣬�õ�������Һ
�۳���ʢ�м�ʯ�ҵ�U�ܵ��������õ�b g
�ܴӷ�Һ©������6 mol��L-1�����ᣬֱ�����ٲ�������Ϊֹ
�ݴӵ���A����������һ�����Ŀ���
���ٴγ���ʢ�м�ʯ�ҵ�U�ܵ��������õ�c g
���ظ�����ݺ͢IJ�����ֱ��U�ܵ������������䣬Ϊd g
����պͻش����⣺
��1������������ƽ������Ʒʱ�������ƽ��ָ������ƫת��˵��___________��
��2��װ���и����B��������_______________��
��3���������Һ©���е����ỻ��Ũ����ͬ�����ᣬ���ԵĽ��___________����ƫ�ߡ�ƫ�ͻ䣩��
��4������ݵ�Ŀ����________________����5������ߵ�Ŀ����________________��
��5���������д�������������ļ���ʽΪ____________________��
���𰸡� ��Ʒ�أ������� ��ֹ�����еĶ�����̼��ˮ������U���� ƫ�� �ѷ�Ӧ�����Ķ�����̼ȫ������U���� �жϷ�Ӧ�����Ķ�����̼�Ƿ�ȫ���ų�������U���еļ�ʯ������ ![]()
��������(1)���ڳ���ʱ�������룬������ƽ�ĸܸ�ԭ��������ƫ˵����Ʒ�أ������
�ʴ�Ϊ����Ʒ�أ������
(2)U���еļ�ʯ����Ϊ�����շ�Ӧ���ɵĶ�����̼����������Ҳ���ڶ�����̼�������B�����þ��Ƿ�ֹ�����еĶ�����̼��ˮ�ֽ���U�ܣ��Խ���������ʴ�Ϊ����ֹ�����е�CO2��ˮ������U���У�
(3)����������лӷ��ԣ�Ҳ�����Ŷ�����̼����U�ܣ�������Ϊ�Ƕ�����̼�����Զ�����̼������ƫ�������̼���Ƶ�����Ҳ��ƫ��ģ����Խ����ƫ�ʴ�Ϊ��ƫ�ߣ�
(4)���ڷ�Ӧ������ƿ�д����ж�����̼������һ�����Ŀ������ǽ������Ķ�����̼��ȫ����U�ܣ��ʴ�Ϊ���ѷ�Ӧ������CO2ȫ������U���У�
(5)ֱ��U�ܵ������������䣬˵��������̼�Ѿ���ȫ���ŵ�U���У��ʴ�Ϊ���жϷ�Ӧ������CO2�Ƿ�ȫ���ų�������U���еļ�ʯ�����գ�
(6)����Ҫ̼���Ƶ�����ΪX����
Na2CO3+H2SO4�TNa2SO4+H2O+CO2��
106 44
X d-b
�б���ʽ![]() ��
��![]() �����X=
�����X=![]() �����������д�������������ļ���ʽΪ
�����������д�������������ļ���ʽΪ![]() ��100%���ʴ�Ϊ��
��100%���ʴ�Ϊ�� ![]() ��100%��
��100%��


 ������������Ӧ����ϵ�д�
������������Ӧ����ϵ�д� ͬ����չ�Ķ�ϵ�д�
ͬ����չ�Ķ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ������������ǣ� ��
A.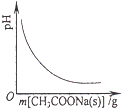 ��CH3COOH��Һ������CH3COONa�������ҺpH�ı仯
��CH3COOH��Һ������CH3COONa�������ҺpH�ı仯
B.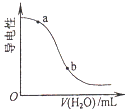 ��CH3COOH��Һ�м�ˮʱ��Һ�ĵ����Ա仯����CH3COOH��Һ��pH��a��b
��CH3COOH��Һ�м�ˮʱ��Һ�ĵ����Ա仯����CH3COOH��Һ��pH��a��b
C.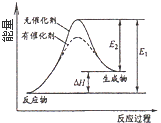 �����ܸı仯ѧ��Ӧ���ʱ�
�����ܸı仯ѧ��Ӧ���ʱ�
D.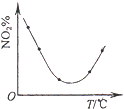 ����NO2���ݻ���ͬ�ĺ����ܱ������У���ͬ�¶��·ֱ�����Ӧ��2NO2��g��N2O4��g������ͬʱ�����NO2���������ߣ���÷�Ӧ�ġ�H��0
����NO2���ݻ���ͬ�ĺ����ܱ������У���ͬ�¶��·ֱ�����Ӧ��2NO2��g��N2O4��g������ͬʱ�����NO2���������ߣ���÷�Ӧ�ġ�H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������ͼ��ʾװ�ý���NaHCO3�����ȷֽ�ʵ�顣��ش�

��1������һ��ʱ����ձ��й۲쵽��ʵ��������__________________________
��2��ʵ�����ʱ����ȷ������____������ĸ����
A���ȴ�Һ�����Ƴ����ܣ���Ϩ��ƾ���
B����Ϩ��ƾ��ƣ��ٴ�Һ�����Ƴ����ܡ�
���������___________��
��3��NaHCO3���ȷֽ�Ļ�ѧ����ʽ________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܵĴ洢������Ӧ�õ���Ҫƿ����Ŀǰ�����û������о�����Ҫ��������У���λ�⻯��������廯���̼�ʲ��ϡ������⻯��ȣ�
��1��Ti��BH4��2��һ�ֹ���Ԫ�����⻯�ﴢ����ϣ� ��Ti2+��̬����Χ�����Ų�ʽ�ɱ�ʾΪ ��
��BH4���Ŀռ乹��������������������
��2��Һ���Ǹ������ʣ������ܵ��������壬����N2+3H2 ![]() 2NH3ʵ�ִ�������⣮����˵����ȷ����������ѡ��
2NH3ʵ�ִ�������⣮����˵����ȷ����������ѡ��
A.NH3������Nԭ�Ӳ���sp3�ӻ�
B.��ͬѹǿʱ��NH3�е��PH3��
C.[Cu��NH3��4]2+�����У�Nԭ������λԭ��
D.CN���ĵ���ʽΪ[��C����N��]��
��3��2008�꣬Yoon���˷���Ca��C60�����ӽṹ��ͼ1�����ɵ�Ca32C60�ܴ�������H2���ӣ� ��C60���������ڱ���CS2 �� C60�����ӣ�����ԡ��Ǽ��ԡ�����
��1mol C60�����У����ЦҼ���ĿΪ ��
��4��һ����Mg��HԪ����ɵ������ǽ����⻯�ﴢ����ϣ��侧���ṹ��ͼ2��ʾ�������ʻ�ѧʽΪ �� 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����������������ȷ����
A. ��״���£�22.4 L H2O���еķ�����ΪNA
B. ���³�ѹ�£�1.06 g Na2CO3����ˮ���е�Na��������Ϊ0.02 NA
C. ͨ��״���£�NA��CO2����ռ�е����Ϊ22.4 L
D. ���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ԭ��Ӧ�У�ˮ��Ϊ����������(����)
A. C��H2O(g)![]() CO��H2 B. 3NO2��H2O===2HNO3��NO
CO��H2 B. 3NO2��H2O===2HNO3��NO
C. 2Na2O2��2H2O===4NaOH��O2�� D. 2F2��2H2O===4HF��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��A��g��+3B��g��M��g��+N��g������H=��49.0kJmol��1 �� һ�������£������Ϊ2L���ܱ������г���2mol A��6molB�����A��M��Ũ����ʱ��仯������ͼ��ʾ�����������У���ȷ���ǣ� �� 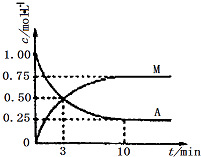
A.��ַ�Ӧ��÷�Ӧ�ų�98 kJ������
B.10min�������¶���ʹ ![]() ����
����
C.3minʱB������������M�������ʵ�3��
D.��Ӧ����ƽ��ʱ��B��ת����Ϊ75%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ������������ȡ������������Ҫ�ɷ�ΪFe2O3��SiO2��Al2O3 �� �������������ʣ���ȡ�̷���FeSO47H2O����������������̣�����˵������ȷ���ǣ� ��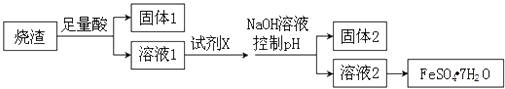
A.�ܽ�����ѡ���������ᣬ�Լ�Xѡ������
B.����1��һ������SiO2 �� ����pH��Ϊ��ʹAl3+ת��ΪAl��OH��3 �� �������2
C.���ı䷽��������Һ1��ֱ�Ӽ�NaOH���������õ��ij����������ܽ⣬����Һ���ᾧ����Ҳ�ɵõ�FeSO47H2O
D.����Һ2�õ�FeSO47H2O��Ʒ�Ĺ����У������������ֹ�������ͷֽ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����п��ع㷺�������ֵ��������ĵ�Դ�����ĵ�ط�Ӧ��Zn+Ag2OH2O=2Ag+Zn��OH��2���Ϸ�����Ӧ�������ǣ� ��
A.Ag
B.Zn��OH��2
C.Ag2O
D.Zn
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com