
某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol·L-1 的MgCl2溶液中各加入10滴2 mol·L-1 NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
|
实验序号 |
加入试剂 |
实验现象 |
|
Ⅰ |
4 mL 2 mol·L-1 HCl 溶液 |
沉淀溶解 |
|
Ⅱ |
4 mL 2 mol·L-1 NH4Cl 溶液 |
沉淀溶解 |
(1)从沉淀溶解平衡的角度解释实验Ⅰ的反应过程 。
(2)测得实验Ⅱ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因 。
(3)甲同学认为应补充一个实验:向同样的Mg(OH)2沉淀中加4 mL蒸馏水,观察到沉淀不溶解。该实验的目的是 。
(4)同学们猜测实验Ⅱ中沉淀溶解的原因有两种:一是NH4Cl溶液显酸性,溶液中的H+可以结合OH- ,进而使沉淀溶解;二是 。
(5)乙同学继续进行实验:向4 mL 2 mol·L-1 NH4Cl溶液中滴加2滴浓氨水,得到pH约为8的混合溶液,向同样的Mg(OH)2沉淀中加入该混合溶液,观察现象。
①实验结果证明(4)中的第二种猜测是成立的,乙同学获得的实验现象是 。
③乙同学这样配制混合溶液的理由是 。
(1)Mg(OH)2(s)  Mg2+(aq)+2OH -(aq)(1分),盐酸中的H+与OH-中和使得OH-浓度减小平衡右移(1分),沉淀溶解
Mg2+(aq)+2OH -(aq)(1分),盐酸中的H+与OH-中和使得OH-浓度减小平衡右移(1分),沉淀溶解
(2)NH4++H2O  NH3·H2O+H+(2分)
NH3·H2O+H+(2分)
(3)排除实验Ⅰ、Ⅱ中(1分)溶剂水使沉淀溶解的可能性(1分)(只答“4 mL水不能使沉淀溶解”给1分)
(4)溶液中c(NH4+)较大,NH4+结合OH-使沉淀溶解(2分)
(5)①沉淀溶解(1分) ②混合溶液显碱性,c(H+)非常小(1分,或答“H+不与OH-结合”), c(NH4+)较大(1分,或答“c(NH4+)与NH4Cl溶液接近”)能确定是NH4+结合OH-使沉淀溶解
【解析】
试题分析:(1)Mg(OH)2存在沉淀溶解平衡:Mg(OH)2(s)
 Mg2+(aq)+2OH -(aq),加入HCl后,H+与OH‾反应,使OH‾浓度减小,沉淀溶解平衡向右移动,Mg(OH)2沉淀溶解。
Mg2+(aq)+2OH -(aq),加入HCl后,H+与OH‾反应,使OH‾浓度减小,沉淀溶解平衡向右移动,Mg(OH)2沉淀溶解。
(2)NH4Cl为强酸弱碱盐,NH4+发生水解反应,离子方程式为:NH4++H2O  NH3·H2O+H+
NH3·H2O+H+
(3)实验Ⅰ、Ⅱ加入溶液,水增多,所以该实验的目的是:排除实验Ⅰ、Ⅱ中溶剂水使沉淀溶解的可能性。
(4)NH4+能与OH‾结合,生成弱电解质NH3•H2O,所以溶液中c(NH4+)较大,NH4+结合OH-使沉淀溶解。
(5)①所加的混合液pH约为8,为碱性,所以沉淀溶解,可证明第二种猜测成立。
②混合液pH约为8,显碱性,c(H+)非常小,而NH4+少量溶解,c(NH4+)浓度较大,可确定沉淀溶解的原因是NH4+与OH‾反应,促进沉淀溶解平衡向右移动。
考点:本题考查沉淀溶解平衡、盐类的水解、实验方案的分析。


科目:高中化学 来源: 题型:
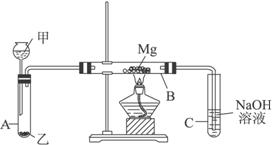
Ⅰ.用如图所示装置进行Mg与SO2反应的实验。
(1)选择制取SO2的合适试剂____________________。
①10%的H2SO4溶液 ②80%的H2SO4溶液 ③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式______________________________。
装置C中NaOH溶液的作用是____________________________________________。
(3)你认为该装置是否有不足之处?__________。如果有,请一一说明____________________。
Ⅱ.某研究小组进行了“实验室制Si”的研究,他们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si。
②Mg在点燃的条件下即可与SiO2反应。
③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
④Si和SiO2均不与稀H2SO4反应。
⑤SiH4在空气中自燃。
他们在研究报告中记载着:“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……再用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右。”
(4)该小组“实验室制Si”的化学方程式是__________。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:

Ⅰ.用如图所示装置进行Mg与SO2反应的实验。
(1)选择制取SO2的合适试剂_________________。
①10%的H2SO4溶液 ②80%的H2SO4溶液 ③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式__________________________ 。装置C中NaOH溶液的作用是__________________。
(3)你认为该装置是否有不足之处?__________。如果有,请一一说明__________________。
Ⅱ.某研究小组进行了“实验室制Si”的研究,他们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si。
②Mg在点燃的条件下即可与SiO2反应。
③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
④Si和SiO2均不与稀H2SO4反应。
⑤SiH4在空气中自燃。
他们在研究报告中记载着:“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制Si”的化学方程式是___________________________。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.用如下化学实验方案的设计及要求—性质、制备和检验图所示装置进行Mg与SO2反应的实验。

(1)选择制取SO2的合适试剂____________________________________________。
①10%的H2SO4溶液 ②98%的H2SO4溶液 ③Na2SO3固体 ④CaSO3固体 ⑤Cu
(2)写出装置B中发生的主要反应的化学方程式___________________________________,
装置C中NaOH溶液的作用是_______________________________________________。
(3)你认为该装置是否有不足之处?________________________________,如果有,请一一说明____________________________________________________________。
Ⅱ.某研究小组进行了“实验室制Si”的研究,它们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si ②Mg在点燃的条件下即可与SiO2反应 ③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4 ④Si和SiO2均不与稀H2SO4反应 ⑤SiH4在空气中自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右”。
(4)该小组“实验室制Si”的化学方程式是_________________________________________。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是_________________
____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知SiO2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性。
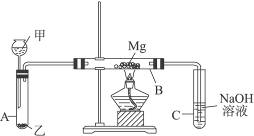
Ⅰ.用如图所示装置进行Mg与SO2反应的实验。
(1)选择制取SO2的合适试剂____________________。
①10%的H2SO4溶液 ②80%的H2SO4溶液 ③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式______________________________。
装置C中NaOH溶液的作用是____________________________________________。
(3)你认为该装置是否有不足之处?__________。如果有,请一一说明____________________。
Ⅱ.某研究小组进行了“实验室制Si”的研究,他们以课本为基础,查阅资料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si。
②Mg在点燃的条件下即可与SiO2反应。
③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
④Si和SiO2均不与稀H2SO4反应。
⑤SiH4在空气中自燃。
他们在研究报告中记载着:“……选用合适的物质在适宜的条件下充分反应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量……再用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预期值的63%左右。”
(4)该小组“实验室制Si”的化学方程式是__________。
(5)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com