
【题目】下列物质中所含化学键类型与其他三种物质不一致的是
A.N2B.H2OC.NaClD.CO2
科目:高中化学 来源: 题型:
【题目】在蒸发皿中加热蒸干下列物质的溶液,再灼烧(溶液低于400℃)可以得到原溶质固体的是
A.AlCl3 B.NaHCO3 C.MgSO4 D.KMnO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是
A. 1 mol FeI2与足量氯气反应时转移的电子数为2NA
B. 常温常压下,46gNO2和N2O4混合气体含有的原子数为3NA
C. 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子数为0.4 NA
D. 常温下56 g铁片投入足量浓H2SO4中生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将燃着的镁条伸入盛有二氧化碳的集气瓶中,镁条继续燃烧,反应的化学方程式为CO2+2Mg ![]() C+2MgO,该反应属于( )
C+2MgO,该反应属于( )
①化合反应 ②分解反应 ③置换反应 ④复分解反应 ⑤氧化还原反应 ⑥离子反应 ⑦非氧化还原反应.
A.①③⑦
B.②③⑥
C.③⑤
D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究化学,不仅要研究化学反应中的物质变化,还要研究伴随着物质变化而发生的能量转化。试回答下列问题:
(1)比较下列各组热化学方程式中△H的大小关系。
已知:S(s)+O2(g)=SO2(g) △H1
S(g)+O2(g)=SO2(g) △H2
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H3
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H4
则△H1______△H2, △H3______△H4 (“>”、“<”或“=”)
(2)煤作为燃料有两种途径:
途径1-直接燃烧:C(s)+O2(g)=CO2(g) △H1<0
途径2-先制水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2>0
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) △H3<0,
2H2(g)+O2(g)=2H2O(g) △H4<0
则△H1、△H2、△H3、△H4的关系式是___________________。
(3)①在298 K、100 kPa下,1 g甲醇完全燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧的热化学方程式为__________________________。
②在甲醇燃烧过程中,当反应中转移1.2mol电子时,燃烧的甲醇的质量为_______g,生成的CO2在标况下的体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。钢铁容易生锈的主要原因是因为钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀。
(1)在空气酸度不大的环境中,其正极反应式为___________________
(2)下列各情况,在其中Fe片腐蚀由快到慢的顺序是___________(用序号表示)。

(3)下图装罝的盐桥中盛有饱和NH4NO3琼脂溶液,能够连接两份电解质溶液,形成闭合回路:

①该装置的能量转化形式为:_________,装置工作时,盐桥中的NH4+移向___________。(“CuSO4溶液”或“AgNO3溶液”)
②若将盐桥换成铜丝,电路中也有电流通过,则铜丝左端为_________极,该极反应式为:___________。
(4)运用原电池原理,设计实验验证Cu2+、Fe3+氧化性的强弱,在下图方框内画出实验装置图_____________(要求:设计一个带盐桥的原电池,标出电极名称及电解质溶液)。该原电池正极反应式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应。已知钠及其氧化物的物质的量均为0.lmol,水的质量为100g。下列说法正确的是

A. Na2O2中阴阳离子数目之比为1:1
B. 反应①的离子方程式为:Na+2H2O=Na++2OH-+H2↑
C. 反应③最多能产生0.05molO2
D. ①、②、③充分反应后所得溶液的质量分数从大到小:①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
如图为实验室某浓硫酸试剂瓶的标签,试根据标签上的有关数据回答下列问题: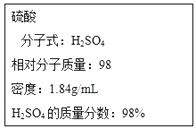
(1)该浓硫酸中H2SO4的物质的量浓度为
(2)某学生欲用上述浓硫酸和蒸馏水配制250mL物质的量浓度为0.4molL﹣1的稀硫酸,该学生需要量取上述浓硫酸进行配制.
(3)为配制(2)中的稀硫酸,下列可供选用的仪器中,一定用到的是(填编号),配制过程中还缺少的仪器是(填写仪器名称)
①玻璃棒;②胶头滴管;③量筒;④药匙;⑤圆底烧瓶;⑥天平;⑦烧杯;⑧普通漏斗
(4)取上述配制好的硫酸溶液50mL与足量的铝反应,所得溶液中c(Al3+)=(忽略溶液体积的变化),检验溶液中SO42﹣存在的方法:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com