
| A�� | ���õķ�ɢϵ��������Һ | |
| B�� | �÷�ɢϵ�ܲ��������ЧӦ | |
| C�� | ���õķ�ɢϵ��ˮ�Ƿ�ɢ�� | |
| D�� | �����÷�ɢϵ���ˣ�����ֽ���ܵõ���ɢ�� |
���� ���ݷ�ɢ����ֱ����С����֪�÷�ɢϵΪ���壬�����ܷ��������ЧӦ��������ֽ���ݴ˷�����
��� �⣺��������������ɢϵ��ɢ������ֱ����5.5-36nm�����ڽ���ķ��룬�߱���������ʣ�
A����ɢ������ֱ����5.5��36nm֮�䣬���÷�ɢϵΪ���壬��A����
B���÷�ɢ�����ڽ��壬�����ж����ЧӦ�����Ե�һ��ǿ��ͨ���˴�����ʱ����ֹ�����ͨ·����B��ȷ��
C�����÷�ɢϵ��ˮ���ɷ�ɢ�ʵ����ʣ����Ƿ�ɢ������C����
D����ɢ�����ڽ��壬����ͨ����ֽ��������ֽ�ϵò�����ɢ�ʣ���D����
��ѡB��
���� ���⿼�齺������ʣ��ѶȲ����ضԻ���֪ʶ�Ĺ��̣�ע��Ի���֪ʶ���������գ�ע�⽺��ı���������


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д� �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 1��2 | C�� | 1��4 | D�� | 1��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | +3 | B�� | +4 | C�� | +5 | D�� | +6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ��Ŀ�� | �Լ������� |
| ֤��̿���к���CuO | |
| ����MgCl2��AlCl3��Һ | |
| ����Na2SO4��CaCO3�������� | |
| ��ȥNaHCO3��Һ�л��е�Na2CO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������Ϊ35����ԭ�ӣ�${\;}_{17}^{35}$Cl | B�� | �Ȼ�淋ĵ���ʽ��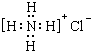 | ||
| C�� | ����Ľṹʽ��H-S-H | D�� | ��������ķ���ʽ��SiO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
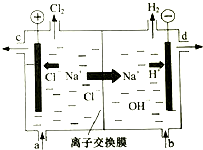 ��ҵ�е��ȼҵ�����ӽ���Ĥ����⾫�Ʊ���ʳ��ˮ����ͼ�����ӽ���Ĥֻ����������ͨ����
��ҵ�е��ȼҵ�����ӽ���Ĥ����⾫�Ʊ���ʳ��ˮ����ͼ�����ӽ���Ĥֻ����������ͨ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
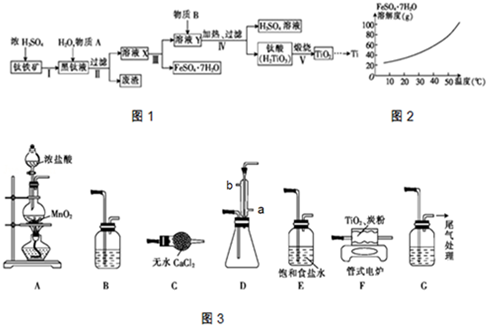
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com