
(15分)工业制纯碱的第一步是通过饱和食盐水、氨和二氧化碳之间的反应,制取碳酸氢钠晶体。该反应原理可以用以下化学方程式表示,已知此反应是放热反应。 NH3+CO2+H2O+NaCl(饱和)= NaHCO3(晶体)↓+NH4Cl
(1)利用上述反应原理,设计如下图所示装置,制取碳酸氢钠晶体.B中盛有饱和碳酸氢钠溶液,C烧杯中盛有冰水,D中装有蘸稀硫酸的脱脂棉,图中夹持装置已略去.制取碳酸氢钠晶体可供选用的药品有:A.石灰石 B.生石灰 C.6mol/L盐酸 D.稀硫酸 E.浓氨水 F.饱和氯化钠溶液。
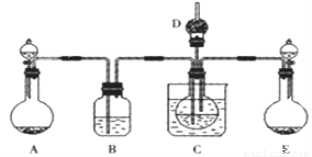
①A中制备气体时,所需药品是(选填字母代号) ;
②B中盛有饱和碳酸氢钠溶液,其作用是 ;
③在实验过程中,向C中通入气体是有先后顺序的,应先通入气体的化学式为 ;
④E装置向C中通气的导管不能插入液面下的原因是 。
(2)该小组同学为了测定C中所得晶体的碳酸氢钠的纯度(假设晶体中不含碳酸盐杂质),将晶体充分干燥后,称量质量为w g。再将晶体加热到质量不再变化时,称量所得粉末质量为m g。然后进行如图所示实验:

①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是(选填字母序号) ;
A.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液
B.在加入氯化钙溶液后,振荡、静置,向溶液中再加入少量碳酸钠溶液
C.在加入氯化钙溶液后,振荡、静置,取上层清液再加入少量碳酸钠溶液
②操作Ⅲ的方法为 、 、 ;
③所得晶体中碳酸氢钠的纯度为 。
(1)①A、C ②除去CO2中的HCl ; ③NH3 ;④防倒吸;
(2)①A ②过滤、洗涤、干燥 ; ③ ( 42n/25w )x100%或84(w-m)/31w。
【解析】
试题分析:(1)①制取CO2是用石灰石和盐酸在烧瓶中发生反应产生的,由于CO2在水中溶解度不大,所以导气管要伸入到液面一下,而制取氨气是将E.浓氨水滴入到盛有B.生石灰的烧瓶中反应制取的,氨气在水中非常容易溶解,所以导气管要在液面上,根据在C中导气管的长短可知:在A中制备CO2气体,所需药品是A、C; ②用盐酸制取CO2气体时,由于盐酸有挥发性,所以其中含有杂质HCl,在 B中盛有饱和碳酸氢钠溶液,其作用就是除去CO2中的杂质HCl ; ③CO2在水中的溶解度小,产生的HCO3-的浓度也就小,不容易形成NaHCO3的饱和溶液,所以难形成沉淀,因此在实验过程中,向C中通入气体应先通入气体的化学式为NH3;④E装置向C中通气的导管不能插入液面下是为了防止倒吸现象的发生;(2)①在操作Ⅱ中,为了判断加入氯化钙溶液是否过量,其中正确的是A.在加入氯化钙溶液后,振荡、静置,向溶液中继续加入少量氯化钙溶液,若不出现白色沉淀,就证明氯化钙溶液过量,否则若产生白色沉淀,就证明氯化钙溶液不足量。因此选项是A。②操作Ⅲ的方法为过滤、洗涤、干燥;③方法一、2NaHCO3 Na2CO3+H2O+ CO2↑,根据方程式可知2×84g =168gNaHCO3完全分解,会产生106g Na2CO3,固体质量会减轻2×84g-106g=62g;现在固体质量减轻(w-m)g,所以其中含有的NaHCO3的质量是[2×84(w-m)÷62] g=84/31(w-m)g.所以所得晶体中碳酸氢钠的纯度为[84(w-m)/31w];方法二:2NaHCO3
Na2CO3+H2O+ CO2↑,根据方程式可知2×84g =168gNaHCO3完全分解,会产生106g Na2CO3,固体质量会减轻2×84g-106g=62g;现在固体质量减轻(w-m)g,所以其中含有的NaHCO3的质量是[2×84(w-m)÷62] g=84/31(w-m)g.所以所得晶体中碳酸氢钠的纯度为[84(w-m)/31w];方法二:2NaHCO3 Na2CO3+H2O+ CO2↑,Na2CO3+CaCl2=CaCO3↓+2NaCl。根据方程式可得关系式:2NaHCO3~Na2CO3~CaCO3;若含有168g NaHCO3,发生反应会产生CaCO3沉淀100g,现在产生沉淀ng,所以原固体中含有NaHCO3的质量是(168n÷100)g,所以NaHCO3的质量分数是[(168n÷100)g÷w g]×100%= ( 42n/25w )x100%。
Na2CO3+H2O+ CO2↑,Na2CO3+CaCl2=CaCO3↓+2NaCl。根据方程式可得关系式:2NaHCO3~Na2CO3~CaCO3;若含有168g NaHCO3,发生反应会产生CaCO3沉淀100g,现在产生沉淀ng,所以原固体中含有NaHCO3的质量是(168n÷100)g,所以NaHCO3的质量分数是[(168n÷100)g÷w g]×100%= ( 42n/25w )x100%。
考点:考查纯碱的制取过程、原理及物质纯度的计算的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届浙江省高二下学期期中考试化学试卷(解析版) 题型:选择题
下图表示4-溴-1-环己醇所发生的4个不同反应。产物只含有一种官能团的反应是( )
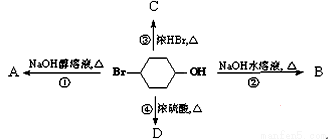
A.②③ B.①④ C.①②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015届浙江省“温州八校”高三返校联考化学试卷(解析版) 题型:选择题
部分氧化的Fe?Cu合金样品(氧化产物为Fe2O3、CuO)共5.76 g,经如下处理:

下列说法正确的是
A.滤液A中的阳离子为Fe2+、Fe3+、H+ B.样品中CuO的质量为4.0 g
C.V=448 D.原样品中Fe元素的质量分数为41%
查看答案和解析>>
科目:高中化学 来源:2015届河南长葛第三实验高中高二下学期第一次考试化学试卷(解析版) 题型:选择题
下列各组物质中,属于同分异构体的是( )
A. 和
和 
B.H2N-CH2-COOH 和 H3C-CH2-NO2
C.CH3-CH2-CH2-COOH 和 H3C-CH2-CH2-CH2-COOH
D.H3C-CH2-O-CH2-CH3 和 
查看答案和解析>>
科目:高中化学 来源:2015届河南省高三上学期第一次测试化学试卷(解析版) 题型:选择题
对某些离子的检验及结论一定正确的是( )
A.加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,则原溶液中一定有SO42-
B.通入Cl2后,溶液变为黄色,加入淀粉后溶液变蓝,则原溶液中一定有I-
C.加入碳酸钠溶液有白色沉淀生成,再加盐酸,沉淀消失,则原溶液中一定有Ba2+
D.加入NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液一定有NH4+
查看答案和解析>>
科目:高中化学 来源:2015届河南省顶级名校高三入学定位考试化学试卷(解析版) 题型:实验题
(12分)设计CO2高温下与木炭反应生成CO的实验。
(1)在右面方框中,A表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置,连接胶管及尾气处理不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如右:
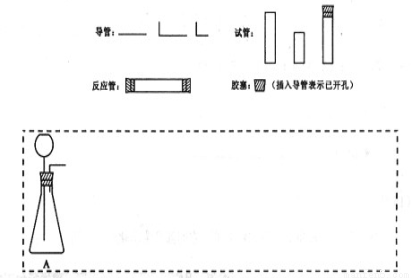
(2)根据方框中的装置图,在答题卡上填写该表
仪器符号 | 仪器中所加物质 | 作用 |
A | 石灰石、稀盐酸 | 石灰石与盐酸生成CO2 |
|
|
|
|
|
|
|
|
|
|
|
|
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是 ;
(4)验证CO的方法是 。
查看答案和解析>>
科目:高中化学 来源:2015届河南省顶级名校高三入学定位考试化学试卷(解析版) 题型:选择题
下列实验设计及其对应的离子方程式均正确的是
A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ = Cu2+ + 2Fe2+
B.Na2O2与H2O反应制备O2 :Na2O2 + H2O = 2Na+ + 2OH- + O2↑
C.将氯气溶于水制备次氯酸:Cl2 + H2O = 2H+ + Cl- + ClO-
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO4- + 6H+ + 5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高三第一次调研考试化学试卷(解析版) 题型:选择题
下列溶液中的Cl-浓度与50 mL 1 mol·L-1 MgCl2溶液中的Cl-浓度相等的是( )
A.150 mL 1 mol·L-1 NaCl溶液
B.75 mL 2 mol·L-1 CaCl2溶液
C.150 mL 2 mol·L-1 KCl溶液
D.75 mL 1 mol·L-1 AlCl3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com