
| A����c(SO42-)=1.05��10-5mol/L��BaSO4��Һ�м���BaSO4���壬c(SO42-)���� |
| B����ñ�����Һ�м���Ba(NO3)2���壬��BaSO4���ܶȻ��������� |
| C����ñ�����Һ�м���Na2SO4���壬�����Һ��c(Ba2+)>c(SO42-) |
| D����ñ�����Һ�м���BaCl2���壬�����Һ��c(SO42-)��С |
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Ag+(aq)��Cl��(aq)�ܽ�ƽ�⣬�ֽ������Ȼ����ֱ����ͬ���µģ���100mL����ˮ�У���100mL0.1mol��L��1�����У���100mL0.1mol��L��1�Ȼ�����Һ�У���100mL0.1mol��L��1�Ȼ�þ��Һ�С���ֽ����������Ũ���ɴ�С��˳����
Ag+(aq)��Cl��(aq)�ܽ�ƽ�⣬�ֽ������Ȼ����ֱ����ͬ���µģ���100mL����ˮ�У���100mL0.1mol��L��1�����У���100mL0.1mol��L��1�Ȼ�����Һ�У���100mL0.1mol��L��1�Ȼ�þ��Һ�С���ֽ����������Ũ���ɴ�С��˳����| A���٢ڢۢ� | B���ۢܢ٢� | C���٢ڢܢ� | D���ۢܢڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
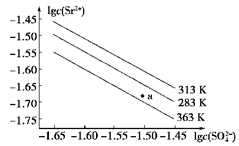
| A���¶�һ��ʱ��Ksp(SrSO4)��c(SO42��)���������С |
| B��������ͬ�¶��У�313 KʱKsp(SrSO4)��� |
| C��283 Kʱ��ͼ��a���Ӧ����Һ�DZ�����Һ |
| D��283 K�µ�SrSO4������Һ���µ�363 K���Ϊ��������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
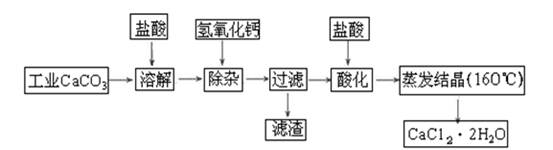 ��1�����Ӳ����Ǽ����������ƹ��壬������Һ��pHΪ8.0~8.5���Գ�ȥ��Һ�е�����Al3+��Fe3+������Fe��OH��3�Ƿ������ȫ��ʵ�������_____________________________________
��1�����Ӳ����Ǽ����������ƹ��壬������Һ��pHΪ8.0~8.5���Գ�ȥ��Һ�е�����Al3+��Fe3+������Fe��OH��3�Ƿ������ȫ��ʵ�������_____________________________________
 ______________��
______________�� 11mol3��L-3,����¶��±��͵�Mg(OH)2��Һ��pHΪ ��
11mol3��L-3,����¶��±��͵�Mg(OH)2��Һ��pHΪ ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��25��Cʱ������Mg(OH)2��Һ�뱥��MgF2��Һ��ȣ�ǰ�ߵ�c(Mg2+)�� |
| B��25��Cʱ����Mg(OH)2������Һ����������NH4Cl���壬c(Mg2+)���� |
| C��25��Cʱ��Mg(OH)2������20mL0.01 mol��L-1��ˮ�е�Ksp����20mL0.01mol��L-1NH4Cl��Һ�е�KspС |
| D��25��Cʱ����Mg(OH)2������Һ�м���NaF��Һ��Mg(OH)2������ת��ΪMgF2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�� 6; 6��10-7 mol��L��1 | B�� 7; 1��10-5 mol��L��1 |
| C��7 ; 4��10-8 mol��L��1 | D�� 6; 1�� 10-5 mol��L��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 �����������ʺ��ܽ���������
�����������ʺ��ܽ����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��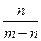 | B��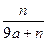 | C��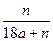 | D��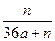 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com