
【题目】阿伏加德罗常数的值为NA.下列说法正确的是( )
A. 1L0.1molL﹣1NH4Cl溶液中,NH4+的数量为0.1NA
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1NA
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2NA
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】实验室需要0.10 mol/L的硫酸920mL,某同学欲用密度为1.84 g/cm![]() 、溶质的质量分数为98%的浓硫酸进行稀释配制。试回答:
、溶质的质量分数为98%的浓硫酸进行稀释配制。试回答:
(1)需选用_______容量瓶(填序号)
A. 50mL B. 100 mL C. 250 mL D. 1000 mL
(2)98%浓硫酸的浓度为_______mol/L (提示:用浓度和密度的换算公式计算) ,需量取浓硫酸______ml。
(3)若提供如下仪器:A. 量筒 B. 托盘天平 C. 玻璃棒 D. 容量瓶 E. 胶头滴管 F. 烧杯
完成该实验需选用仪器_______________(将仪器标号填在横线上)。
(4)下列操作会使所配制的溶液物质的量浓度一定偏低的是___________。
A. 容量瓶底部有蒸馏水 B. 向容量瓶转移溶液时,有少量液体溅出 C. 加水时,水量超过了刻度线
(5)下列关于容量瓶的使用方法中,正确的是__________________(填序号)。
A. 使用前要检验是否漏水 B. 在容量瓶中直接溶解固体或稀释液体
C. 溶液未经冷却即注入容量瓶中 D. 向容量瓶中转移溶液可以不用玻璃棒引流
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验溶液中是否含有某种离子,下列操作方法正确的是 ( )
A. 某溶液加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,则一定含有CO32一
B. 某溶液加入氢氧化钠溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝,则一定含有NH4+
C. 某溶液滴入BaCl2溶液,再滴加稀盐酸,产生白色沉淀,则一定含有SO42一
D. 某溶液加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则一定含有Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫和钙的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)钙元素的焰色反应呈砖红色,其中红色对应的辐射波长为_____(填字母)nm。
A.435 B500 C.580 D.605 E. 700
(2)元素S和Ca中,第一电离能较大的是_____(填元素符号),其基态原子核外电子排布式为_______。
(3)X射线衍射测定等发现,石膏(CaSO4 2H2O)中存在SO42-离子。SO42-离子的几何构型为_____,中心原子的杂化形式为________。
(4) 基态Ca原子中,核外电子占据最高能层的符号是____,占据该能层电子的电子云轮廓图形状为_____。钙元素和锰元素属于同一周期,且核外最外层电子构型相同,但金属钙的熔点、沸点等都比金展锰低,原因是_________________。
(5)过氧化钙晶体的晶胞结构如图所示,已知该晶胞的密度是ρ g cm-3,则晶胞结构中最近的两个Ca2+间的距离为______ (列算式即可,用NA表示阿伏加德罗常数的数值)nm,与Ca2+紧邻O22-的个数为______。
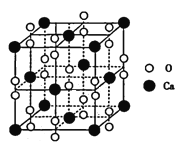
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 标准状况下,22.4 L H2SO4中含有6.02×1023个硫原子
B. 常温常压下,16g O2中含有6.02×1023个氧原子
C. 500mL 0.5mol·L-1的Fe2(SO4)3溶液中SO42-浓度为0. 75 mol·L-1
D. 0.5mol OH-中含有3.01×1023个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液中大量共存的是
A.Ba2+ NO32- K+ SO42-B.Fe3+ OH- Cl- Na+
C.H+ Na+ CO32- Cl-D.Na+ K+ Cl- NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z三种主族元素在元素周期表中的位置如图所示。设X的原子序数为a,则下列说法不正确的是( )

A. Y的原子序数可能为a-17 B. Y与Z的原子序数之和可能为2a
C. Z的原子序数可能为a+31 D. X、Y、Z可能为短周期元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示,下列说法正确的是

A. 原溶液中含有的Fe3+和Al3+的物质的量之比为1 : 1
B. 原溶液中一定含有SO42-和Na+
C. 反应最后形成的溶液中含有的溶质为Na2SO4
D. 原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com