
 H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���
H2(g)+CO2(g)����Ӧ�����вⶨ�IJ������ݼ��±���| ��Ӧʱ��/min | 0 | 2 | 4 | 6 |
| n(CO)/mol | 1.20 | 0.90 | | 0.80 |
| n(H2O)/ mol | 0.60 | | 0.20 | |

| ��� | ҩƷ1 | ҩƷ2 | ʵ������ |
| I | 0.01 mol/L NaOH��Һ | 0.01 mol/L MgCl2��Һ | ���ɰ�ɫ���� |
| II | 0.01 mol/L��ˮ | 0.01 mol/L MgCl2��Һ | ������ |
| III | 0.1 mol/L��ˮ | 0.1 mol/L MgCl2��Һ | ����III |
| IV | 0.1 mol/L��ˮ | 0.01 mol/L MgCl2��Һ | ���ɰ�ɫ���� |
| V | 0.01 mol/L��ˮ | 0.1 mol/L MgCl2��Һ | ������ |
 2NH4+(aq) + Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK= ���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ ��
2NH4+(aq) + Mg(OH)2(s)�÷�Ӧ��ѧƽ�ⳣ���ı���ʽΪK= ���г��÷�Ӧƽ�ⳣ��K��Kb(NH3��H2O)��Ksp(Mg(OH)2)�Ĺ�ϵʽ �� ��2�֣�
��2�֣� ��
��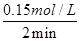 ��0.075 mol��L��1��min��1��
��0.075 mol��L��1��min��1�� H2(g)+CO2(g)
H2(g)+CO2(g) ��1.0
��1.0 ��
�� ��K��
��K�� ��Kb2/Ksp��
��Kb2/Ksp��

 ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺
2NH3(g) ��H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺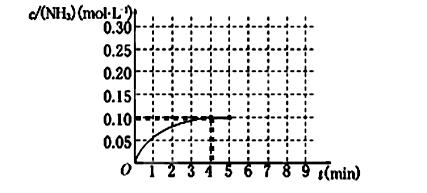
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3CH2OH(g)����ͼ����ϩ��ת�������¶ȡ�ѹǿ�ı仯��ϵ������˵����ȷ���ǣ� ��
CH3CH2OH(g)����ͼ����ϩ��ת�������¶ȡ�ѹǿ�ı仯��ϵ������˵����ȷ���ǣ� ��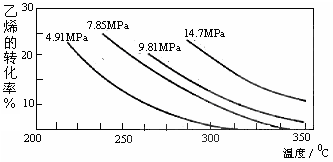
| A���÷�ӦΪ���ȷ�Ӧ |
| B����ҵ�ϲ���7MPa���ң�250��300�棬���ۺϿ��Ƿ�Ӧ���ʺ��Ҵ��IJ��ʵ����صĽ�� |
| C����ͬ�¶��£�ѹǿԽ����ϩ��ת����Խ��ƽ�ⳣ��Խ�� |
| D�������㹻��ѹǿ���ʵ����¶ȣ���ʵ����ϩ��ת����Ϊ 100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�
C(g)+D(g)��Ӧ��ƽ�ⳣ�����¶ȵĹ�ϵ���£�| �¶�/�� | 700 | 900 | 830 | 1000 | 1200 |
| ƽ�ⳣ�� | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 A(g)+B(g)��ƽ�ⳣ����ֵΪ___________________��
A(g)+B(g)��ƽ�ⳣ����ֵΪ___________________�� 2P��g��+Q��s����Ӧ�����±�����Ͷ�ϣ���Ӧ�ﵽƽ��״̬�������ϵѹǿ���ߣ������÷�Ӧ��ƽ�ⳣ�����¶ȵı仯��ϵ��__________________________________________________________________________________��
2P��g��+Q��s����Ӧ�����±�����Ͷ�ϣ���Ӧ�ﵽƽ��״̬�������ϵѹǿ���ߣ������÷�Ӧ��ƽ�ⳣ�����¶ȵı仯��ϵ��__________________________________________________________________________________��| �� �� | M | N | P | Q |
| ��ʼͶ��/mol | 2 | 1 | 2 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
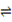 CH3OH(g)+H2O(g) ��H <0 ��500 ��ʱ�������Ϊ1 L�Ĺ̶��ݻ����ܱ������г���1mol CO2��3mol H2�����CO2Ũ����CH3OH Ũ����ʱ��ı仯��ͼ��ʾ�����еó��Ľ��۴������
CH3OH(g)+H2O(g) ��H <0 ��500 ��ʱ�������Ϊ1 L�Ĺ̶��ݻ����ܱ������г���1mol CO2��3mol H2�����CO2Ũ����CH3OH Ũ����ʱ��ı仯��ͼ��ʾ�����еó��Ľ��۴������
| A������X���Ա�ʾCH3OH(g) ��H2O(g) ��Ũ�ȱ仯 |
| B���ӷ�Ӧ��ʼ��10minʱ��H2�ķ�Ӧ����v(H2)=0.225mol/(L�qmin) |
| C��ƽ��ʱH2��ת����Ϊ75% |
| D��500 ��ʱ�÷�Ӧ��ƽ�ⳣ��K=3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
|


 ��1����֪��Ӧһ������������Ͻ����ͻᴦ�ں���״̬��д�����������Ļ�ѧ����ʽ��______________________________________________�����¶�����ʱ���÷�Ӧ��ƽ�ⳣ��Kֵ___________(���������С�����䡱)��
��1����֪��Ӧһ������������Ͻ����ͻᴦ�ں���״̬��д�����������Ļ�ѧ����ʽ��______________________________________________�����¶�����ʱ���÷�Ӧ��ƽ�ⳣ��Kֵ___________(���������С�����䡱)�� 2NH3���÷�Ӧ�ڹ̶��ݻ����ܱ������н��С����и����־�Ÿ÷�Ӧ�ﵽ��ѧƽ��״̬����____________(�����)
2NH3���÷�Ӧ�ڹ̶��ݻ����ܱ������н��С����и����־�Ÿ÷�Ӧ�ﵽ��ѧƽ��״̬����____________(�����)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO2(g)+H2(g)��CO��ת���ʺ��¶�t�Ĺ�ϵ���±���
CO2(g)+H2(g)��CO��ת���ʺ��¶�t�Ĺ�ϵ���±���| t(��) | 750 | 850 | 1000 |
| CO% | 0.7 | 2/3 | 0.5 |
 CH3OH(g)+H2O(g) ��H��-49.0 kJ��mol��1���������Ϊ1 L���ܱ������У�����
CH3OH(g)+H2O(g) ��H��-49.0 kJ��mol��1���������Ϊ1 L���ܱ������У�����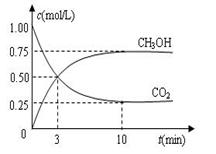
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
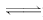 CH3OH��g����
CH3OH��g����
 cC��g��+ dD��g��������ͼ�ش�
cC��g��+ dD��g��������ͼ�ش�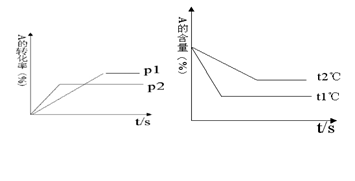
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ѧ��Ӧ����v | B��ˮ�����ӻ�����Kw |
| C����ѧƽ�ⳣ��K | D������ĵ���ƽ�ⳣ��Ka |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com