
| A. | 黄绿色的氯水光照后颜色变浅 | |
| B. | 在硫酸亚铁溶液中,加入铁粉以防止氧化变质 | |
| C. | 生产硝酸的过程中使用过量空气以提高氨气的利用率 | |
| D. | 实验室常用排饱和食盐水的方法收集氯气 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动,使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.Cl2+H2O?HCl+HClO,次氯酸见光分解,平衡正向移动,氯气浓度减小,颜色变浅,能用勒夏特列原理解释,故A不选;
B:在硫酸亚铁易被氧化为硫酸铁,而铁粉可充分将硫酸铁还原为硫酸亚铁,不能用平衡移动原理解释,故B选;
C:硝酸生产的第一步为氨的催化氧化4NH3+5O2?4NO+6H2O,通过通往过量的空气而增大氧气浓度使平衡右移,增大氨气的转化率,可以用平衡移动原理解释,故C不选;
D:氯气在水中存在平衡:Cl2+H2O?H++Cl-+HClO,而将氯气通入饱和食盐水中,相当于增加了氯离子浓度,平衡左移,减少氯气的溶解,可以用平衡移动原理解释,故D不选;
故选B.
点评 本题考查化学平衡移动原理,为高频考点,明确平衡移动原理内涵及其适用范围是解本题关键,只有改变条件时能引起可逆反应平衡移动的才能用平衡移动原理解释,题目难度不大.


科目:高中化学 来源: 题型:解答题
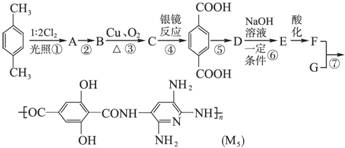
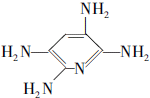 ,F的含氧官能团的名称有酯基和酚羟基.
,F的含氧官能团的名称有酯基和酚羟基.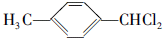 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 可逆反应A(?)+aB(g)?C(g)+D(g).反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )
可逆反应A(?)+aB(g)?C(g)+D(g).反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )| A. | 若a=1,则A为液体或固体 | |
| B. | 该反应正反应为放热反应 | |
| C. | T2>T1,p2>p1 | |
| D. | 其他条件不变,增加B的物质的量,化学平衡向正反应方向移动,化学平衡常数K增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
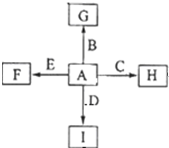 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
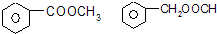 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2FeO4在净水过程中能转变成氢氧化铁 | |
| B. | Na2FeO4能杀菌消毒 | |
| C. | Na2FeO4能除去水中的硫化氢等还原性气体杂质 | |
| D. | Na2FeO4能吸附水中的颜色和固体颗粒 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
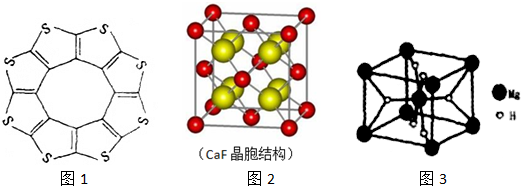
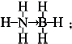 ;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).
;与氨硼烷互为等电子体的有机小分子是CH3CH3(写结构简式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com