
【题目】燃料电池是利用燃料(如CO、H2、CH4等)与氧气反应,将反应产生的化学能转变为电能的装置,通常用氢氧化钾作为电解质溶液.完成下列关于甲烷(CH4)燃料电池的填空:
(1)甲烷与氧气反应的化学方程式为:________.
(2)已知燃料电池的总反应式为CH4+2O2+2KOH═K2CO3+3H2O,电池中有一极的电极反应为CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O,这个电极是燃料电池的(填“正极”或“负极”),另一个电极上的电极反应式为:
(3)随着电池不断放电,电解质溶液的碱性(填“增大”、“减小”或“不变”)
【答案】
(1)
CH4+2O2 ![]() CO2+2H2O
CO2+2H2O
(2)负极;2O2+4H2O+8e﹣═8OH﹣
(3)减小
【解析】(1)甲烷在氧气中燃烧生成二氧化碳和水,反应方程式为CH4+2O2![]() CO2+2H2O,所以答案为:CH4+2O2
CO2+2H2O,所以答案为:CH4+2O2![]() CO2+2H2O;(2)CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O中C元素化合价由﹣4价变为+4价,所以甲烷失电子发生氧化反应,其所在电极为负极,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为2O2+4H2O+8e﹣═8OH﹣ , 所以答案为:负极;2O2+4H2O+8e﹣═8OH﹣;(3)该燃料电池电池反应式为CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O,氢氧根离子参加反应,所以反应过程中氢氧根离子浓度减小,溶液的pH减小,所以答案为:减小.
CO2+2H2O;(2)CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O中C元素化合价由﹣4价变为+4价,所以甲烷失电子发生氧化反应,其所在电极为负极,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为2O2+4H2O+8e﹣═8OH﹣ , 所以答案为:负极;2O2+4H2O+8e﹣═8OH﹣;(3)该燃料电池电池反应式为CH4+10OH﹣﹣8e﹣═CO32﹣+7H2O,氢氧根离子参加反应,所以反应过程中氢氧根离子浓度减小,溶液的pH减小,所以答案为:减小.
本题考查了燃料电池,根据得失电子确定正负极发生的反应,能正确书写电极反应式.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】有机物G是一种医药中间体,常用于制备抗凝血药.可以通过如下所示的合成路线合成有机物G. 
已知:
①RCOOH ![]() RCOCl
RCOCl
②  +NaOH→
+NaOH→ ![]() +H2O
+H2O
请回答下列问题:
(1)写出A中官能团的名称: .
(2)D的结构简式: .
(3)写出B→C的化学反应方程式: .
(4)下列说法正确的是(填选项)
A.有机物G的分子式为C9H8O3
B.F能使酸性KMnO4溶液褪色
C.甲酸甲酯与C互为同分异构体
D.有机物A,B,C均能溶解于水.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠硫电池属于温绿色二次电流,用液态钠、硫和多硫化钠作电极,以能传导钠离子的固体氧化铝作电解质.电池反应为:2Na+xS ![]() Na2Sx . 下列有关说法正确的是( )
Na2Sx . 下列有关说法正确的是( )
A.放电时,Na+向负极移动
B.放电时,正极上发生的反应为xS+2Na++2e﹣=Na2Sx
C.充电时,阳极上发生的反应为2Na﹣2e﹣=2Na+
D.放电时,每有0.4mol电子转移,则有9.2gNa和6.4g硫参加反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以苯为主要原料,采用以下合成路线合成医药中间体G和可降解聚合物C.
已知:2CH3CHO ![]() CH2CH(OH)CH2CHO
CH2CH(OH)CH2CHO ![]() CH2CH=CHCHO
CH2CH=CHCHO
(1)写出X的结构式
(2)对于高分子化合物C的说法正确的是 . (填序号)
A.1molC能与2n molNaOH反应
B.(C9H8O3)n既是高分子化合物C的化学式,也是链节的化学式
C.高分子化合物C是缩聚产物
D.酸性条件下降解时有气泡产生
(3)在一定条件下,E可以生成一种含有3个六元环的化合物(C18H16O4),请写出该反应的化学方程式
(4)写出符合要求的G的同分异构体(含有 ![]() 的有机物不能稳定存在)
的有机物不能稳定存在)
a.遇FeCl3溶液显紫色b.能与Br2按1:2发生加成反应 c.苯环上只有两种等效氢
(5)根据题目所给信息,以F和乙烯为原料,设计合成G的反应路线(用流程图表示,无机试剂任选).
例:CH3CH2OH ![]() H2C=CH
H2C=CH ![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子能大量共存的是( )
A.含大量H+的溶液中:CrO42-、Cl-、NO3-、Na+
B.含大量AlO2-的溶液中:Na+、K+、NO3-、HCO3-
C.含大量Al3+的溶液中:Na+、K+、NO3-、ClO-
D.含大量CH3COO-的溶液中:NH4+、Cl-、F-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,已知H2CO3H++HCO3﹣K1=4.3×l0﹣7;
HCO3﹣H++CO32﹣K2=5.6×l0﹣11;
H2OH++OH﹣Kw=1.0×l0﹣14
现取10.6g Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )
A.W点所示的溶液中:c(Na+)+c(H+)=2c(CO32﹣)+c(OH﹣)+c(HCO3﹣)
B.pH=4的溶液中:c(H2CO3)+c(HCO3﹣)+c(CO32﹣)=0.1 molL﹣1
C.pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3﹣)=c(OH﹣)+c(Cl﹣)
D.pH=11的溶液中:CO32﹣+H2OHCO3﹣+OH﹣K=1.8×l0﹣4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.
(1)一定温度下,向固定体积为2L的密闭容器中充入SO2和NO2各1mol,发生反应SO2(g)+NO2(g)SO3(g)+NO(g),测得上述反应5min末到达平衡,此时容器中NO与NO2的体积比为3:1,则这段时间内SO2的反应速率υ(SO2)= , 此反应在该温度下的平衡常数K= .
(2)甲醇日趋成为重要的有机燃料,通常利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示: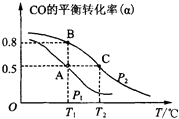
①上述合成甲醇的反应为反应(填“放热”或“吸热”).
②A、B、C三点的平衡常数KA、KB、KC的大小关系为 . A、B两点对应的压强大小关系是PAPB(填“大于”、“小于”或“等于”).
③若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为 , 理论上通过外电路的电子最多为 mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com