
���������һ�ָ�Ч��ɫˮ���������乤ҵ�Ʊ��ķ�Ӧԭ��Ϊ
2Fe(OH)3 + 3KClO + 4KOH��2K2FeO4 + 3KCl + 5H2O������˵����ȷ����
| A���Ʊ����������ClO?����ԭ�� |
| B���Ʊ��������ʱ1 mol Fe(OH)3�õ�3 mol ���� |
| C��������������Ļ��ϼ�Ϊ+7 |
| D���ø�����ش���ˮʱ���仹ԭ������ˮ���������ǿ���������Ľ��� |
D
�������������A����Ӧ2Fe(OH)3 + 3KClO + 4KOH��2K2FeO4 + 3KCl + 5H2O�У�ClԪ�صĻ��ϼ���+1�۽���Ϊ-1�ۣ���KClOΪ��������Fe(OH)3Ϊ��ԭ������A����B����Ӧ����Ԫ�صĻ��ϼ���+3�����ߵ�+6�ۣ���1mol Fe(OH)3ʧȥ3mol���ӣ���B����C��������������Ļ��ϼ�Ϊ��6�ۣ���C����D���ø�����ش���ˮʱ��+6�������ֳ�ǿ�����ԣ���ɱ���������仹ԭ����Ϊ�����ӣ���ˮ�����������������壬������ˮ�е��������ʣ���D��ȷ����ѡD��
���㣺����������ԭ��Ӧ���й��ж��Լ���̼���ε�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���з�Ӧ��Ҫ��������������ʵ�ֵ���
| A��Cl2��Cl- | B��H+ ��H2 | C��MnO2 ��Mn2+ | D��Zn��Zn2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ͬλ��ʾ�ٷ������ڷ�Ӧ�������о������з�Ӧ�У�ͬλ��ʾ�ٱ�ʾ��ȷ����
| A��CH3COOH+C2H18 5OH��CH3COOC2H5+H18 2O |
B��NH4Cl+2H2O NH3��2H2O+HCl NH3��2H2O+HCl |
| C��K37ClO3+6HCl=K37Cl+3Cl2��+3 H2O |
| D��2KMnO4+5H218O2+3H2SO4=K2SO4+2MnSO4+518O2��+8H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��NaIO3�ļ�����Һ��ͨ�����������Եõ�Na2H3IO6�������йظ÷�Ӧ��˵���������
| A���ڸ÷�Ӧ��NaIO3����ԭ�� |
| B�����������£�����������ǿ��Na2H3IO6 |
| C����Ӧ������1mol Na2H3IO6��ת��2mol���� |
| D����Ӧ�����������뻹ԭ��������ʵ�����Ϊ2:1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪Co2O3��������Һ���ױ���ԭ��Co2+��Co2O3��Cl2��FeCl3��I2���������μ��������з�Ӧ��ˮ��Һ�в����ܷ�������
| A��Co2O3 + 6 HCl��2CoCl2 + Cl2��+ 3H2O |
| B��Cl2 + FeI2 = FeCl2 + I2 |
| C��3 Cl2 + 6 FeI2 = 2FeCl3 + 4 FeI3 |
| D��2Fe3+ + 2I�� = 2Fe2++ I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ͼΪ��ӦFe + CuSO4 ==FeSO4 + Cu�е���ת�ƵĹ�ϵͼ����ͼ�е�Ԫ�ؼס��ҷֱ��ʾ
| A��Fe Cu | B��Cu S | C��Fe O | D��Fe S |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪����ԭ��HSO3¯>I¯��������IO3¯> I2���ں�3 mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ��������ͼ��ʾ����������ȷ���ǣ� ��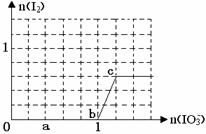
| A��0~b ��3HSO3��+ IO3���� 3SO4����+ I��+ 3H�� |
| B��a��ʱ����NaHSO3�����ʵ���Ϊ1��2 mol |
| C��b~c��I2�ǻ�ԭ���� |
| D������Һ��I¯��I2�����ʵ���֮��Ϊ5��2ʱ�������KIO3Ϊ1��8mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�����£���������Һ�з������·�Ӧ
��16H++10Z-+2XO4-��2X2++5Z2+8H2O ��2A2+ +B2��2A3++2B-
��2B-+Z2��B2+2Z-
�ɴ��ж�����˵��������ǣ� ��
| A����ӦZ2+2A2+��2A3++2Z-���Խ��С� |
| B����ԭ����ǿ������˳����A2+��B-��Z-��X2+ |
| C����������ǿ������˳����XO4-��Z2��B2��A3+ |
| D��ZԪ���ڢ٢۷�Ӧ�о�����ԭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪2Al��2NaOH��2H2O 2NaAlO2��3H2���÷�Ӧ���й���������������ȷ���ǣ�NA��ʾ�����ӵ�������
2NaAlO2��3H2���÷�Ӧ���й���������������ȷ���ǣ�NA��ʾ�����ӵ�������
| A��ÿ����0.3 mol H2������ԭ��ˮ������ĿΪ0.6 NA |
| B������2.7 g Al�μӷ�Ӧʱ��ת�Ƶĵ�����ĿΪ0.3 NA |
| C��ÿ����6.72 L��H2����Һ��AlO2������Ŀ������0.2 NA |
| D����Һ��ÿ����0.1 mol��AlO2����Na������Ŀ������0.1 NA |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com