
【题目】某化学兴趣小组同学用实验室中一瓶久置的NaOH固体做了以下实验:先称取13.3 g NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入浓度为4 mol/L的盐酸,再根据生成CO2的体积计算出Na2CO3的质量,从而进一步计算出样品中变质NaOH的质量
请回答下列问题:
(1)该实验的目的是_________________
(2)已知20 ℃时,Na2CO3溶解度为21.7 g ,NaOH溶解度为108.3 g若要将所称取的样品恰好溶解,最多需要蒸馏水____________g,溶解样品所需的仪器是_____________________
(3)实验测得加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:

则13.3 g 该样品中未变质的NaOH的质量为____________;NaOH的变质程度为_________(用质量分数表示);与NaOH反应消耗的盐酸体积为________mL
(4)根据“与NaOH反应消耗盐酸的体积”,并对照上述图像,他们从实验中还发现了什么问题?_____________________,并由此得出了什么结论?_______________ ____________
【答案】(1)测定NaOH的变质程度
(2)61.3 烧杯玻璃棒量筒
(3)8.00g 33.3% 50.0
(4)NaOH被盐酸中和后继续滴加盐酸未立即产生气体 CO32-![]()
【解析】
试题分析:(1)根据题目叙述,该实验的目的是测定NaOH的变质程度;
(2)已知20 ℃时,Na2CO3溶解度为21.7 g ,NaOH溶解度为108.3 g利用极值法,若要将所称取的样品恰好溶解,最多需要蒸馏水xg,![]() 得到X=61.3g
得到X=61.3g
溶解样品所需的仪器是烧杯玻璃棒量筒(3)由图可知,生成二氧化碳为1.12L,则:
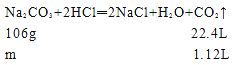
m(Na2CO3)=![]() =5.3g
=5.3g
故样品中氢氧化钠的质量=13.3g-5.3g=8g
根据![]() ,
,
生成5.3g碳酸钠需要氢氧化钠4g,NaOH的变质程度为![]() 33.3%
33.3%
(2)8g氢氧化钠的物质的量=![]() =0.2mol,则:
=0.2mol,则:
![]()
氢氧化钠消耗盐酸的体积=![]() =0.05L=50mL。
=0.05L=50mL。
(4)根据“与NaOH反应消耗盐酸的体积”,并对照上述图像从实验中还发现NaOH被盐酸中和后继续滴加盐酸未立即产生气体,说明![]() 、
、![]() 分步进行。
分步进行。


科目:高中化学 来源: 题型:
【题目】(1)3.6g H2O物质的量为 mol ,约含有 个电子;与3.6g H2O所含H个数相同的CH4 的质量是 ,标准状况下体积约是 。
(2)标准状况下,容积为VmL的烧瓶内充满NH3,设NA代表阿伏加德罗常数的数值。
①标准状况下NH3的密度是 ,烧瓶内氢原子总数是 。
②已知NH3极易溶于水,所得溶液称为氨水(溶质为NH3)。用烧瓶中的NH3做喷泉实验,水充满烧瓶,所得溶液密度为d g/mL,假设NH3没有损耗,所得溶液物质的量浓度为 mol/L,溶质的质量百分数为 。
③标准状况下该烧瓶若充满H2时总质量为a g ,则充满NH3时烧瓶总质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中有Fe3+、Mg2+、Fe2+和Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并充分搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
A.Fe3+ B.Mg2+ C.Fe2+ D.Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则加入铝粉质量为( )
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如下图所示。则下列离子组在对应的溶液中,一定能大量共存的是( )

A. a点对应的溶液中:Na+、OH-、SO![]() 、NO
、NO![]()
B. b点对应的溶液中:Al3+、Fe3+、MnO![]() 、Cl-
、Cl-
C. c点对应的溶液中:Na+、Ca2+、NO![]() 、Cl-
、Cl-
D. d点对应的溶液中:F-、NO![]() 、Fe3+、Ag+
、Fe3+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离物质的方法中,不正确的是( )
A. 利用分馏的方法从石油中分离出汽油和煤油
B. 利用分液的方法将水和酒精分离
C. 利用结晶的方法除去硝酸钾中混有的少量氯化钠
D. 利用过滤的方法除去水中的泥沙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年中美专家研制出可在一分钟内完成充电的超常性能铝离子电池,分别以金属铝和石墨为电极,用A1C14-、A12C17-和有机阳离子组成电解质溶液,其放电工作原理如下图所示。下列说法不正确的是( )
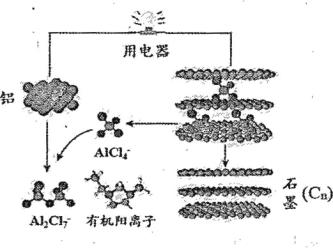
A.放电时,铝为负极、石墨为正极
B.充电时的阳极反应为:Cn+ A1C14- - e-= Cn A1C14
C.放电时的负极反应为:Al-3e- +7 A1C14-=4A12C17-
D.放电时,有机阳离子向铝电极方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)被称为21世纪的新型能源,它清洁、高效、具有优良的环保性能。
I.Ⅰ.工业制备二甲醚的生产流程如下:

催化反应室中(压力2.0~10.0Mpa,温度230~280℃)发生如下反应:
CO(g)+2H2(g)![]() CH3OH(g)△H=-90.7kJ/mol ①
CH3OH(g)△H=-90.7kJ/mol ①
2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol ②
CH3OCH3(g)+H2O(g)△H=-23.5kJ/mol ②
CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=-41.2kJ/mol ③
CO2(g)+H2(g)△H=-41.2kJ/mol ③
(1)甲烷氧化可制得合成气,反应如下:CH4(g)+![]() O2
O2![]() CO(g)+2H2(g) △H=-35.6kJ/mol。该反应是_______反应(填“自发”或“非自发”)
CO(g)+2H2(g) △H=-35.6kJ/mol。该反应是_______反应(填“自发”或“非自发”)
(2)催化反应室中总反应3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g)的△H=______,830℃时反应③的K=1.0,则在催化反应室中反应③的K______1.0(填“>”、“<”或“=”)。
CH3OCH3(g)+CO2(g)的△H=______,830℃时反应③的K=1.0,则在催化反应室中反应③的K______1.0(填“>”、“<”或“=”)。
(3)上述反应中,可以循环使用的物质有________。
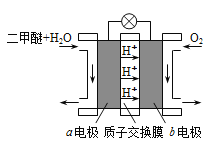
II.如图为绿色电源“二甲醚燃料电池”的工作原理示意图。b 电极是______极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com