
科目:高中化学 来源:不详 题型:单选题
| A.第一步通过浓硫酸,第二步通过无水氯化钙 |
| B.第一步通过碱石灰,第二步通过浓硫酸 |
| C.第一步通过饱和食盐水, 第二步通过无水氯化钙 |
| D.第一步通过水,第二步通过氧化钙 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
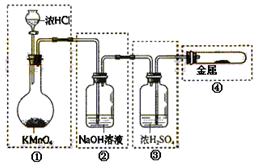
| A.只有①和②处 |
| B.只有②处 |
| C.只有②和③处 |
| D.只有②、③、④处 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
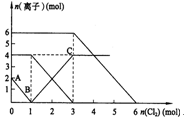
| A.还原性:I— >Fe2+>Br— |
| B.原混合溶液中FeBr2的物质的量为6mol |
| C.当通入2molCl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 HCl + HClO K=4.5×10-4
HCl + HClO K=4.5×10-4 地控制次氯酸的浓度,请结合平衡常数解释原因: 。
地控制次氯酸的浓度,请结合平衡常数解释原因: 。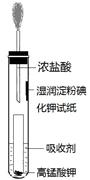
| A.饱和食盐水 | B.饱和Na2SO3溶液 |
| C.饱和NaOH溶液 | D.浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 应,制得氯气0.56L(标准状况)。问:
应,制得氯气0.56L(标准状况)。问:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
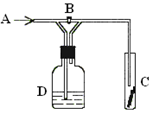
| A.浓H2SO4 | B.饱和NaCl溶液 |
| C.浓NaOH溶液 | D.浓NaBr溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 5C1—+ ClO3+3H2O。该兴趣小组设计了下列实验装置,进行实验。
5C1—+ ClO3+3H2O。该兴趣小组设计了下列实验装置,进行实验。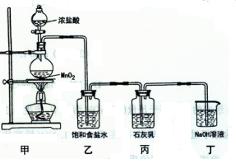
 的化学方程式是 , 乙装置的作用是 。
的化学方程式是 , 乙装置的作用是 。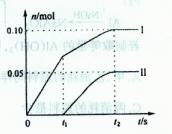
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。
5Cl-+ClO3-+3H2O。该兴趣小组设计了下列实验装置,进行实验。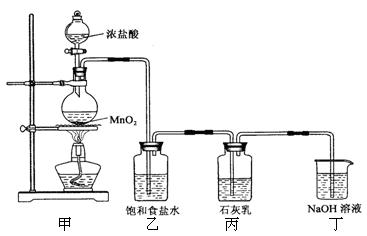
 制得Ca(ClO)2______________g。
制得Ca(ClO)2______________g。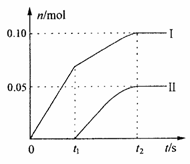
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com