
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
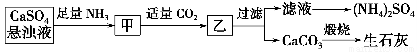
下列推断不合理的是 ( )。
A.生成1 mol(NH4)2SO4至少消耗2 mol NH3
B.CO2可被循环使用
C.往甲中通CO2有利于(NH4)2SO4的生成
D.直接蒸干滤液即可得到纯净的(NH4)2SO4
科目:高中化学 来源:2014年江苏省南通市业水平测试(必修)化学试卷(解析版) 题型:选择题
⑴促进生态文明,保护生态环境,是实现“中国梦”的重要组成部分。
① 生活中一次性物品的使用会大大增加生态压力,一次性纸巾使用后应投入贴有 (填字母)标志的垃圾桶内。



a b c
② 用明矾处理废水中细小悬浮颗粒的方法属于 (填字母)。
a.混凝法 b.中和法 c.氧化还原法
③ 向燃煤中加入石灰石作为脱硫剂,可以减少煤燃烧时产生的SO2。发生反应的化学方程式为 。
⑵营养平衡、科学使用食品添加剂有助于健康和提高免疫力。
① 医用维生素C片常在药片外包裹一层“糖衣”,其作用除了 改善口感外,更重要的作用是 。
② 某品牌高钙梳打的配料标签如图所示。在所列配料中,富含糖类的是 ,植物油在体内水解最终产物是高级脂肪酸和 。碳酸钙与胃酸反应的离子方程式为 。

⑶材料的不断发展可以促进社会进步。

① “玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金,选用镁铝合金的优点是 (任答一点)。
② 生产玻璃时,纯碱与石英反应的化学方程式为 。碳化硅硬度很大,它属于 (填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
③ 用于包装食品的塑料袋,应选用 (填“聚乙烯塑料”或“聚氯乙烯塑料”),合成该塑料的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十三 有机物结构及同分异构体数目判断练习卷(解析版) 题型:选择题
相对分子质量为100的烃,且含有4个甲基的同分异构体共有(不考虑立体异构)( )。
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十七 化学工艺流程题练习卷(解析版) 题型:填空题
为了提高资源利用率,减少环境污染,化工集团将钛厂、氯碱厂和甲醇厂组成产业链,如图所示。

请填写下列空白:
(1)钛铁矿进入氯化炉前通常采取洗涤、粉碎、烘干、预热等物理方法处理,请从原理上解释粉碎的作用:_______________________________________;
已知氯化炉中反应氯气和焦炭的理论用料物质的量比为7∶6,则氯化炉中的还原剂化学式是_________________________________________________。
(2)已知:①Mg(s)+Cl2(g)=MgCl2(s) ΔH=-641 kJ·mol-1
②2Mg(s)+TiCl4(s)=2MgCl2(s)+Ti(s) ΔH=-512 kJ·mol-1
则Ti(s)+2Cl2(g)=TiCl4(s) ΔH=________。
(3)Ar气通入还原炉中并不参与反应,通入Ar气的作用是_________________________________________________________________。
(4)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为2CH3OH+3O2+4OH-===2CO32—+6H2O,该电池中正极上的电极反应式为____________________________________________。
工作一段时间后,测得溶液的pH________(填“减小”、“增大”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十一 元素的单质及其化合物的性质与转化练习卷(解析版) 题型:选择题
下列转化关系中,不能通过一步反应实现的是 ( )。
①SiO2→Na2SiO3 ②CuSO4→CuCl2 ③SiO2→H2SiO3 ④CuO→Cu(OH)2 ⑤Na2O2→Na2SO4
A.①和② B.③和④ C.②③④ D.②③④⑤
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十 电解质溶液中微粒浓度的关系练习卷(解析版) 题型:选择题
常温下,在10 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是 ( )。

A.在0.1 mol·L-1 Na2CO3溶液中:c(Na+)+c(H+)=c(CO32—)+c(HCO3—)+
c(OH-)
B.当溶液的pH为7时,溶液的总体积为20 mL
C.在B点所示的溶液中,浓度最大的阳离子是Na+
D.在A点所示的溶液中:c(CO32—)=c(HCO3—)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练八 化学反应速率和化学平衡分析与判断练习卷(解析版) 题型:选择题
合成氨所需的氢气可用煤和水作原料经过多步反应制得,其中的一步反应为:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0。反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )。
CO2(g)+H2(g) ΔH<0。反应达到平衡后,为提高CO的转化率,下列措施中正确的是( )。
A.增加压强 B.降低温度 C.增大CO的浓度 D.更换催化剂
查看答案和解析>>
科目:高中化学 来源:2014年化学高考课时演练10甲烷乙烯苯煤石油天然气的综合利用练习卷(解析版) 题型:填空题
下表是A、B、C、D、E五种有机物的有关信息:
A①能使溴的四氯化碳溶液褪色;
②比例模型为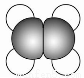
③能与水在一定条件下反应生成C
B①由C、H两种元素组成。
②球棍模型为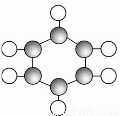
C①由C、H、O三种元素组成;
②能与Na反应;
③与E反应生成相对分子质量为88的酯
D①相对分子质量比C少2;
②能由C催化氧化得到
E①由C、H、O三种元素组成;
②其水溶液能使紫色石蕊试液变红
回答下列问题:
(1)A~E中,属于烃的是___________(填字母)。
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为_______________。
(3)C催化氧化生成D的化学方程式为_________________________________。
(4)有机物B具有的性质是__________ (填序号)。
①无色无味的液体;②有毒;③不溶于水;④密度比水大;⑤能使酸性KMnO4溶液和溴水褪色
(5)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是________________________(用化学方程式说明)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com