
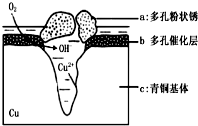
 青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀.如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法不正确的是( )
青铜器的制造是中华民族劳动人民智慧的结晶,成为一个时代的象征,但出土的青铜器大多受到环境腐蚀.如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图.环境中的 Cl- 扩散到孔口,并与各电极产物作用生成多孔粉状锈 Cu2 ( OH )3 Cl.下列说法不正确的是( )| A. | 腐蚀过程中,负极 b 被氧化 | |
| B. | 环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl↓ | |
| C. | 若生成 2.145gCu 2 ( OH ) 3 Cl,则理论上消耗标准状况氧气体积为 0.448L | |
| D. | 正极的电极反应式为:正极反应是 O2+4e-+2H2O=4OH- |
分析 A、根据图知,氧气得电子生成氢氧根离子、Cu失电子生成铜离子,发生吸氧腐蚀,则Cu作负极被氧化;
B、多孔粉状锈 Cu2 ( OH )3 Cl为固体,不能拆;
C、n[Cu2(OH)3Cl]=$\frac{4.29g}{214.5g/mol}$=0.02mol,根据转移电子计算氧气物质的量,再根据V=nVm计算体积;
D、氧气得电子生成氢氧根.
解答 解:A、根据图知,氧气得电子生成氢氧根离子、Cu失电子生成铜离子,发生吸氧腐蚀,则Cu作负极被氧化,腐蚀过程中,负极是c,故A选;
B、多孔粉状锈 Cu2 ( OH )3 Cl为固体,故生 成 Cu 2( OH )3 Cl 的 离子方程式为:2Cu2++Cl-+3OH-═Cu 2( OH )3Cl,故B不选;
C、n[Cu2(OH)3Cl]=$\frac{4.29g}{214.5g/mol}$=0.02mol,根据转移电子得n(O2)=$\frac{0.02mol×2×2}{4}$=0.02mol,故在标准状态体积为V=0.02mol×22.4L/mol=0.448L,故C不选;
D、氧气在正极得电子生成氢氧根离子,电极反应式为:O2+4e-+2H2O=4OH-,故D不选;
故选A.
点评 本题考查了原电池原理及电极反应式、电池反应式的书写及其计算,难度中等,掌握原理是解题关键.


科目:高中化学 来源: 题型:选择题
| A. | 用稀硫酸和锌粒反应制取氢气时加入少许硫酸铜粉末以加快反应速率 | |
| B. | 向乙酸乙酯中加入饱和碳酸钠溶液以除去乙酸乙酯中少量的乙酸 | |
| C. | 向盛有沸水的烧杯中滴加FeC13饱和溶液并长时间煮沸以制取Fe(OH)3胶体 | |
| D. | 向蔗糖中滴加浓硫酸可证明浓硫酸有脱水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
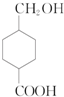 .M的同分异构体有多种,符合下列条件的同分异构体有( )
.M的同分异构体有多种,符合下列条件的同分异构体有( )| A. | 9种 | B. | 10种 | C. | 11种 | D. | 12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaH、NH3都属于共价化合物 | B. | 12C、C60都属于碳的同素异形体 | ||
| C. | 水玻璃、硅酸都属于胶体 | D. | 生铁、青铜都属于合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
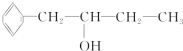
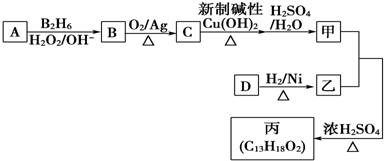
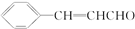 ;
;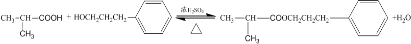 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 诗句 | 相关物质 | 相关说法 |
| A | 春蚕到死丝方尽 | 纤维素 | 高分子化合物 |
| B | 蜡炬成灰泪始干 | 脂肪烃 | 不饱和烃 |
| C | 沧海月明珠有泪 | 碳酸钙 | 强电解质 |
| D | 蓝田日暖玉生烟 | 二氧化硅 | 两性氧化物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取a g混合物用酒精灯充分加热后质量减少b g | |
| B. | 取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收后质量增加b g | |
| C. | 取a g混合物与足量氢氧化钡溶液充分反应,过滤、洗涤、烘干,得b g固体 | |
| D. | 取a g混合物于锥形瓶中加水溶解,滴入1~2滴酚酞指示剂,用标准盐酸溶液滴定至终点,消耗盐酸V mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物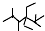 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 分子式为C5H12O的醇,能在铜催化下被O2氧化为醛的同分异构体有4种 | |
| C. | 1 mol乙酸在浓H2SO4存在下与足量乙醇反应可得1 mol乙酸乙酯 | |
| D. | 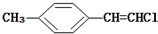 分子中的所有原子有可能共平面 分子中的所有原子有可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
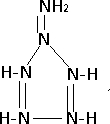 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com