
已知钡的金属活动性处于钾和钠之间。则下列变化中可能实现的是
A.钡可从氯化钠溶液中置换出金属钠
B.钡可从冷水中置换出氢气
C.钡可从硫酸铜溶液中置换出铜
D.在溶液中Ba2+可氧化金属锌,生成Zn2+
科目:高中化学 来源:2016届广西河池市高三上学期第一次月考理综化学试卷(解析版) 题型:填空题
(15分)开发、使用清洁能源发展“低碳经济”正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:
①2CH3OH(l)+3O2(g)= 2CO2(g)+4H2O(g)ΔH1=-1275.6 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g)ΔH2=-566.0 kJ·mol-1
③H2O(g)=H2O(l)ΔH3=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(2)生产甲醇的原料CO和H2来源于: CH4(g)+H2O(g)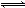 CO(g)+3H2(g)ΔH>0
CO(g)+3H2(g)ΔH>0
①该反应的平衡常数表达式K= ,一定条件下CH4的平衡转化率与温度、压强的关系如图a。则T1 T2(填“<”“>”或“=”下同),A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为___________。
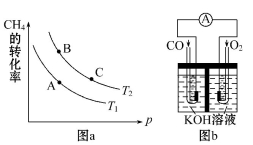
②120℃时,将1 mol CH4和2 mol H2O(g)通入容积为1 L的密闭容器中发生反应,不能说明该反应已经达到平衡状态的是 。
a.容器内气体密度恒定
b.混合气体的相对分子质量恒定
c.容器内的压强恒定
d.3v正(CH4)=v逆(H2)
e.单位时间内消耗0.3 mol CH4同时生成0.9mol H2
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,则该电池负极的电极反应式为 。当有4mol电子通过导线时,消耗标准状况下的O2体积为 L ,此时电解质溶液的PH值 (填“变大”、“变小”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省太原市高一上入学考试化学试卷(解析版) 题型:选择题
具备基本的化学实验技能是进行科学探究的基本保证。下列实验操作中正确的是( )
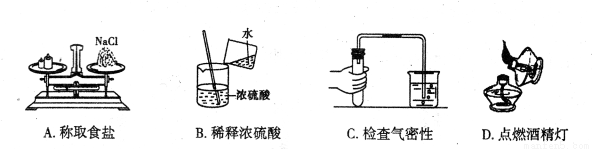
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省合肥市高二上开学考试化学试卷(解析版) 题型:填空题
(5分)麻醉剂的发现和使用,是人类医疗史上了不起的一项成就,它可使患者在接受治疗中感觉不到疼痛。
(1)一种常用的麻醉剂氯仿(CHCl3),常因保存不善被氧化而变质,产生剧毒物光气(COCl2)。
2CHCl3+O2 2HCl+2COCl2.为防止发生事故,使用前可用于检验是否变质的试剂是(填序号)________。
2HCl+2COCl2.为防止发生事故,使用前可用于检验是否变质的试剂是(填序号)________。
A.淀粉碘化钾溶液 B.NaOH溶液
C.酚酞溶液 D.硝酸酸化的硝酸银溶液
(2)稀有气体氙气(Xe)在医疗上很受重视,常常作为麻醉剂,氙气能溶于细胞的油脂里,引起细胞麻醉和膨胀,从而神经末梢作用暂时停止。人们曾试用体积分数为80%氙气和20%的氧气组成的混合气体,作为无副作用的麻醉剂。氙在元素周期表中位于_______周期,______族,它的原子序数是______。
(3)作为稀有气体,氙的化学性质不活泼,但它可在一定条件下生成化合物。取1molXe和3.5mol氟气于一密闭容器内充分反应,后来余下了1.5mol的氟气同时有白色固体生成,此白色固体的化学式为_________。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省等六校教研会高三第一次联考化学试卷(解析版) 题型:填空题
煤炭是我国的主要能源之一,与之伴生的二氧化硫(SO2)和酸雨污染问题较为突出。目前我国采用的控制方法是电厂烟气脱硫。烟气脱硫的原理是利用碱性物质吸收并固定酸性的二氧化硫,主要有如下两种方法:
I、钠碱循环法脱硫技术。
(1)此法是利用Na2SO3溶液可脱除烟气中的SO2。Na2SO3可由NaOH溶液吸收SO2制得,该反应的离子方程式: 。
(2)NaOH溶液吸收SO的过程中,pH随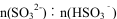 变化关系如下表:
变化关系如下表:

①由上表判断,NaHSO3溶液显 性,用化学平衡原理解释: 。
②当溶液呈中性时,离子浓度关系正确的是(选填字母): 。
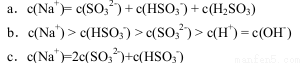
II、石灰石脱硫法
此法是以石灰石为原料通过系列反应将硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
CaSO4 (s)+ CO (g) CaO(s)+ SO2 (g)+ CO2 (g) △H=218.4kJ·mol-1(反应Ⅰ)
CaO(s)+ SO2 (g)+ CO2 (g) △H=218.4kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g) CaS(s)+ 4CO2(g) △H2= -175.6kJ·mol-1 (反应Ⅱ)
CaS(s)+ 4CO2(g) △H2= -175.6kJ·mol-1 (反应Ⅱ)
请回答下列问题:
(1)结合反应Ⅰ、Ⅱ写出CaSO4(s)与CaS(s)的热化学反应方程式 。
(2)对于气体参与的反应,表示平衡常数 Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则反应Ⅰ的Kp= (用表达式表示)。
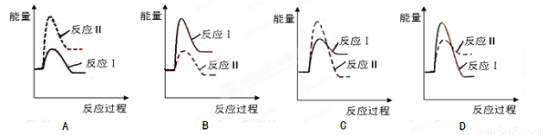
(3)假设某温度下,反应Ⅰ的速率(v1)小于反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是 。
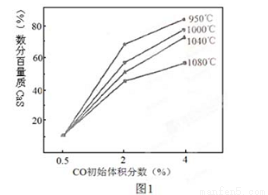
(4)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数 的关系曲线。则降低该反应体系中产生的SO2生成量的措施有 。
A、向该反应体系中投入生石灰
B、在合适的温度区间内控制较低的反应温度
C、降低CO的初始体积百分数
D、提高反应体系的温度
查看答案和解析>>
科目:高中化学 来源:2016届安徽省等六校教研会高三第一次联考化学试卷(解析版) 题型:选择题
下列有关仪器的使用方法或实验操作正确的是
A、做金属钠与水反应实验时,剩余的钠不能再放入原试剂瓶
B、酸式滴定管装标准液前,必须先用该溶液润洗
C、锥形瓶用作反应容器时一定不能加热
D、用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高三普通班8月月考化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.向FeCl2溶液中通入氯气:Fe2+ + Cl2 = Fe3+ + 2Cl-
C.向Ca(ClO)2溶液中通入过量的SO2:C1O- + SO2 + H2O=HClO + HSO3-
D.FeSO4酸性溶液中加H2O2:2Fe2++H2O2=2Fe3++2OH-
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期四调考试化学试卷(解析版) 题型:填空题
(10分)纳米级Cu2O是优良的催化剂和半导体材料,工业上常用下列方法制备Cu2O。
(1)热还原法:加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为________________________________。
(2)电解法:以氢氧燃料电池为电源,用电解法制备Cu2O装置如图所示。
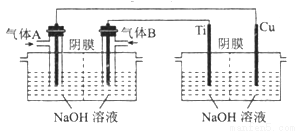
①A的化学式为___________________________。
②燃料电池中,OH-的移动方向为______________(填“由左向右”或“由右向左”);电解池中,阳极的电极反应式为____________________________。
③电解一段时间后,欲使阴极室溶液恢复原来组成,应向其中补充一定量的_____________(填化学式)。
④制备过程中,可循环利用的物质为________________(填化学式)。
(3)干法还原法
利用反应Cu+CuO Cu2O也可制备Cu2O。将反应后的均匀固体混合物(含有三种成分)等分为两份,一份与足量H2充分反应后,固体质量减少6.4g;另一份恰好溶于500mL稀硝酸,生成标准状况下4.48LNO,该稀硝酸的物质的量浓度为_________________。
Cu2O也可制备Cu2O。将反应后的均匀固体混合物(含有三种成分)等分为两份,一份与足量H2充分反应后,固体质量减少6.4g;另一份恰好溶于500mL稀硝酸,生成标准状况下4.48LNO,该稀硝酸的物质的量浓度为_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com