
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | 5.9 |
| 完全沉淀的pH | 3.2 | 8.8 | 8.9 |
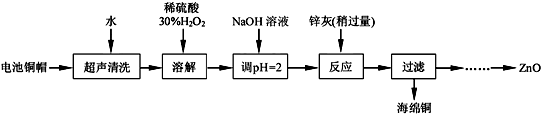
分析 利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收 Cu并制备ZnO,电池铜帽加入水过滤后除去溶于水的杂质,在固体中加入过氧化氢溶解,铜生成硫酸铜溶液,加热煮沸将溶液中过量的H2O2除去,加入氢氧化钠溶液调节溶液PH=2沉淀铁离子,加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物),反应过滤得到海绵铜,沉淀锌离子得到氢氧化锌,分解得到氧化锌,
(1)①酸性条件下Cu与过氧化氢发生氧化还原反应生成硫酸铜和水;
②过氧化氢加热到153℃便猛烈的分解;
(2)①根据淀粉与碘单质作用变蓝解答;
②根据H2O2+2I-+2H+=I2+2H2O解答;
(3)滴加H2O2溶液,使Fe2+转化完全为Fe3+,滴加NaOH溶液,形成氢氧化铁沉淀,除杂后形成氢氧化锌沉淀,过滤、洗涤、干燥900℃煅烧制得氧化锌.
解答 解:利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收 Cu并制备ZnO,电池铜帽加入水过滤后除去溶于水的杂质,在固体中加入过氧化氢溶解,铜生成硫酸铜溶液,加热煮沸将溶液中过量的H2O2除去,加入氢氧化钠溶液调节溶液PH=2沉淀铁离子,加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物),反应过滤得到海绵铜,沉淀锌离子得到氢氧化锌,分解得到氧化锌,
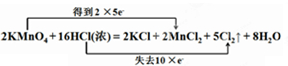
(1)①因为双氧水在酸性溶液中先把铜氧化成氧化铜,当然这是一个微弱的反应,形成一个平衡,但是形成的氧化铜马上就会被稀硫酸溶解,平衡被打破,反应朝正方向进行,故而逐渐溶解,反应的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O;
故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O;
②过氧化氢性质比较稳定,若加热到153℃便猛烈的分解为水和氧气,将溶液中过量的H2O2 除去可加热至沸,
故答案为:加热至沸;
(2)①淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点,
故答案为:淀粉溶液;蓝色褪去并半分钟内不恢复;
②若留有H2O2,加入KI后,会有以下反应:H2O2+2I-+2H+=I2+2H2O,误当成2Cu2++4I-=2CuI(白色)↓+I2 生成的碘,使测定结果偏高,
故答案为:偏高;
(3)根据表中阳离子沉淀的PH可知,由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入30%H2O2,使其充分反应,目的使Fe2+转化完全为Fe3+,②加氢氧化钠溶液,控制PH在4左右,使Fe3+沉淀完全,③过滤,向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全,⑤过滤、洗涤、干燥;
⑥900℃煅烧,制得氧化锌,
故答案为:①向滤液中加入略过量30%的H2O2,使其充分反应;②向反应后的溶液中滴加1.0 moL•L-1的NaOH溶液,调节溶液的pH约为5(或3.2≤pH<5.9);④向滤液中滴加1.0 moL•L-1的氢氧化钠,调节pH约为10(或8.9≤pH≤11).
点评 本题主要考查物质的回收、制备,为高考常见题型,侧重考查学生对综合实验处理能力,注意实验方案的设计原理和步骤是解答的关键,平时注意打好扎实的基础知识和灵活应用知识解决问题的能力培养,题目难度中等.


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol•L-1的乙醇溶液中分子总数为0.1NA | |
| B. | 常温常压下,28 g乙烯含有的电子数为16NA | |
| C. | 44g乙酸乙酯和丁酸的混合物中共含有碳原子数为2 NA | |
| D. | m g丙烯和戊烯的混合物中共用电子对数为$\frac{3m}{14}$NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 400 | 500 | 600 |
| SO2转化率/% | 99.2 | 93.5 | 73.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C(s)+O2(g)═CO(g);△H=-393.5 kJ/mol | |
| B. | 2H2(g)+O2(g)═2H2O(g);△H=+571.6 kJ/mol | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(g);△H=-890.3 kJ/mol | |
| D. | $\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2 (g)+3H2O(l);△H=-1400 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
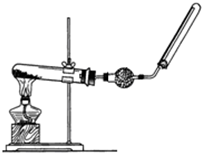 实验室中若用如图所示的装置制取并收集干燥的氨气.
实验室中若用如图所示的装置制取并收集干燥的氨气.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用已知浓度NaOH溶液滴定未知浓度盐酸,滴定终点时,俯视刻度线,则测得盐酸浓度偏小 | |
| B. | 用新制氢氧化铜悬浊液可以鉴别乙酸、葡萄糖和淀粉三种溶液 | |
| C. | 通常采用产生气泡的快慢,来比较不同条件下Na2S2O3溶液与稀硫酸的反应速率 | |
| D. | 受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液或饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
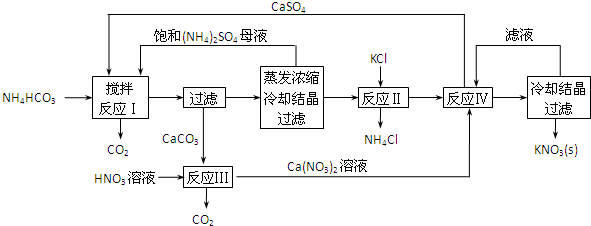
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
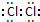 ;
;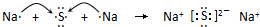 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com