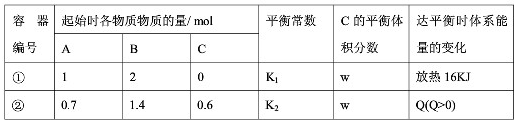
分析:A.由达平衡时①放出的热为46.3kJ,计算平衡时XY
3的物质的量,再根据v=
计算v(XY
3);
B.恒温恒容下,②中按化学计量数转化到左边,满足n(X
2)=1mol,n(Y
2)=3mol,两平衡是完全等效平衡,据此解答;
C.由达平衡时①放出的热为46.3kJ,计算平衡时X
2、Y
2和XY
3的物质的量,分析②是否处于平衡状态或是向哪个方向进行,判断②是吸热还是放热;
D.从平衡移动的角度比较反应放出的热量与46.3kJ的关系.
解答:解:A.2min达平衡时,①放出的热为46.3kJ,则平衡时XY
3的物质的量为2mol×
=1mol,故v(XY
3)=
=
mol?L
-1?s
-1,故A正确;
B.恒温恒容下,②中按化学计量数转化到左边,n(X
2)=0.4mol+1.2mol×
=1mol,n(Y
2)=1.2mol+1.2mol×
=3mol,两平衡是完全等效平衡,故平衡时XY
3的浓度相等为
=4mol/L,故B正确;
C.①容器中放出46.3kJ热量,则生成氨气的物质的量为:2mol×
=1mol,则:
?N
2(g)+3H
2(g)
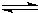
2NH
3(g)
起始:1mol 3mol 0
转化:0.5mol 1.5mol 1mol
平衡:0.5mol 1.5mol 1mol
由上述计算,可知平衡时①容器中X
2、Y
2和XY
3的物质的量分别为0.5mol、1.5mol和1mol,②与①为完全等效平衡,所以,平衡时②容器中X
2、Y
2和XY
3的物质的量也分别为0.5mol、1.5mol和1mol,可知②的反应向逆反应方向进行,反应过程需要吸收热,故C正确;
D.若容器①体积为0.3L,减小压强平衡向逆反应方向移动,反应物的转化率降低,达平衡时放出的热量小于46.3kJ,故D错误;
故选D.
点评:本题考查化学平衡移动问题、等效平衡、反应热等问题,题目难度中等,注意C项根据计算分析,注意从等效平衡的角度解答,也可以利用平衡常数解答.

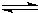 2NH3(g)
2NH3(g)