
【题目】用氟硅酸(H2SiF6)制备冰晶石(Na3AlF6)的工艺流程如下所示:

(1)氟硅酸(H2SiF6)酸性强于硫酸,通常由四氟化硅经水吸收制得,其化学方程式为______________________________。
(2)反应②为脱硅工艺,滤渣②是__________。
(3)向NaF溶液中加入Al2(SO4)3溶液发生反应③的离子方程式为_______________;NaF溶液呈碱性,在加入A l2(SO4)3溶液前,需先用硫酸将NaF溶液的pH下调至5左右,否则可能产生副产物______________。
(4)干燥前,检验冰晶石是否洗涤干净的实验方法是____________________________。
(5)从母液中可循环利用的物质是_____________________。
(6)碳酸化法也是工业制取冰晶石的一种方法:在偏铝酸钠及氟化钠溶液中,通入足量二氧化碳即可,请写出该反应的化学方程式____________________________。
【答案】 3SiF4+3H2O=2H2SiF6+H2SiO3 SiO2 6F-+Al3++3Na+=Na3AlF6↓ Al(OH)3 取洗涤后的溶液,![]() 向其中滴加BaCl2溶液,无现象,说明已经洗涤干净;
向其中滴加BaCl2溶液,无现象,说明已经洗涤干净;![]() 若有白色沉淀生成,说明没有洗涤干净 Na2SO4 6NaF+4CO2+NaAlO2+2H2O=Na3AIF6↓+4NaHCO3
若有白色沉淀生成,说明没有洗涤干净 Na2SO4 6NaF+4CO2+NaAlO2+2H2O=Na3AIF6↓+4NaHCO3
【解析】(1)氟硅酸(H2SiF6)酸性强于硫酸,通常由四氟化硅经水吸收制得,反应的化学方程式为3SiF4+3H2O=2H2SiF6+H2SiO3,故答案为:3SiF4+3H2O=2H2SiF6+H2SiO3;
(2)氟硅酸(H2SiF6)酸性强于硫酸,氟硅酸与硫酸钠溶液反应生成硫酸和氟硅酸钠(Na2SiF6),根据流程图,氟硅酸钠难溶于水,过滤得到的氟硅酸钠与氢氧化钠反应,反应②为脱硅工艺,则反应生成氟化钠和二氧化硅,因此滤渣②是二氧化硅,故答案为:SiO2;
(3)向NaF溶液中加入Al2(SO4)3溶液反应生成Na3AlF6沉淀和硫酸钠,反应③的离子方程式为6F-+Al3++3Na+=Na3AlF6↓;NaF溶液呈碱性,在加入A l2(SO4)3溶液前,需先用硫酸将NaF溶液的pH下调至5左右,否则A l2(SO4)3溶液与碱反应生成氢氧化铝沉淀,故答案为:6F-+Al3++3Na+=Na3AlF6↓;Al(OH)3;
(4)冰晶石上可能吸附硫酸钠溶液,判断是否洗涤干净只需要具有是否含有硫酸根离子即可,实验方法为取洗涤后的溶液,向其中滴加BaCl2溶液,无现象,说明已经洗涤干净;若有白色沉淀生成,说明没有洗涤干净,故答案为:取洗涤后的溶液,向其中滴加BaCl2溶液,无现象,说明已经洗涤干净;若有白色沉淀生成,说明没有洗涤干净;
(5)母液中含有硫酸钠,根据流程图,硫酸钠参与反应①的循环Na2SO4,故答案为:Na2SO4;
(6)在偏铝酸钠及氟化钠溶液中,通入足量二氧化碳可以反应生成Na3AlF6沉淀,反应的化学方程式为6NaF+4CO2+NaAlO2+2H2O= Na3AlF6↓+4NaHCO3,故答案为:6NaF+4CO2+NaAlO2+2H2O= Na3AlF6↓+4NaHCO3。


科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过如图途径制备: 
请回答下列问题:
(1)环戊二烯分子中最多有个原子共平面;
(2)金刚烷的分子式为 , 其分子中的﹣CH2﹣基团有个;其一氯代物有种.
(3)已知烯烃能发生如下的反应: 
![]() RCHO+R′CHO 请写出下列反应产物的结构简式:
RCHO+R′CHO 请写出下列反应产物的结构简式: ![]()
![]() .
.
(4)写出环戊二烯与Br2 发生1,4﹣加成的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见如图。下列说法正确的是( )

A. 此电池在常温时也能工作 B. 正极电极反应式为:O2+2CO2-4e﹣=2CO32﹣
C. CO32﹣向正极移动 D. a为CH4,b为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 马口铁(镀锡)的表面一旦破损,铁腐蚀加快 B. 白铁(镀锌)的表面一旦破损,铁腐蚀加快
C. 用铝质铆钉铆接铁板,铁易被腐蚀 D. 钢铁设备上装上镁合金是阴极保护法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T1℃时,在四个容积均为1L的恒容密闭容器中发生反应:2NO(g)+2H2(g)![]() N2(g)+2H2O(g) ΔH,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n为常数),测得有关实验数据如下:
N2(g)+2H2O(g) ΔH,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n为常数),测得有关实验数据如下:
容器编号 | 物质的起始浓度/(mol/L) | 速率/(mol·L-1·s-1) | 物质的平衡浓度/(mol/L) | |
c(NO) | c(H2) | c(N2) | ||
Ⅰ | 6×10-3 | 1×10-3 | a×10-3 | 2×10-4 |
Ⅱ | 6×10-3 | 2×10-3 | 2a×10-3 | |
Ⅲ | 1×10-3 | 6×10-3 | b×10-3 | |
Ⅳ | 2×10-3 | 6×10-3 | 4b×10-3 | |
下列说法正确的是( )
A. m=2,n=2
B. 达到平衡时,容器Ⅱ与容器Ⅳ的总压强之比为1:2
C. 温度升高为T2℃,测得平衡时,容器Ⅱ中c(H2O)=3.8×10-4mol/L,则ΔH>0
D. T1℃时,容器Ⅲ中达到平衡后再充入NO、H2O(g)各2×10-4mol,则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某无色溶液中含有H+、Mg2+、Al3+几种阳离子,逐滴加入氢氧化钠溶液,消耗氢氧化钠溶液的体积(x轴)和生成沉淀量(y轴)之间的函数关系,正确的是( )
A.
B.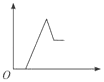
C.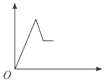
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下两个反应:(A)NaOH+HCl===NaCl+H2O (B)2FeCl3+Cu===2FeCl2+CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)(A)______,(B)________;
(2)如果(A或B)不能,说明其原因_________________________________________;
(3)如果(A或B)可以,则在下面方框中画出装置图并写出正、负极材料及电极反应式
________
负极:________、_______________________________________;
正极:________、________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】试样X由氧化亚铁和氧化铜组成.取质量相等的两份试样按下图所示进行实验: 
(1)请写出步骤③中所发生的全部反应的离子方程式.
(2)若全部的溶液Y和全部的粉末Z充分反应后,生成的不溶物W的质量是m,则每份试样X中氧化铜的质量为 . (用m表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题.氢气、甲醇是优质的清洁燃料,可制作燃料电池. 
(1)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=﹣1275.6kJmol﹣1②2CO(g)+O2(g)=2CO2(g)△H2=﹣566.0kJmol﹣1
③H2O(g)=H2O(l)△H3=﹣44.0kJmol﹣1写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(2)生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)CO(g)+3H2(g) ①一定条件下CH4的平衡转化率与温度、压强的关系如图a.则,P1P2;A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为 . (填“<”、“>”“=”)
②100℃时,将1mol CH4和2mol H2O通入容积为1L 的反应室,反应达平衡的标志是: .
A.容器内气体密度恒定
B.单位时间内消耗0.1mol CH4同时生成0.3mol H2
C.容器的压强恒定
D.3v正(CH4)=v逆(H2)
③如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K=
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为 . 用该原电池做电源,常温下,用惰性电极电解200mL饱和食盐水(足量),消耗标准状况下的CO 224mL,则溶液的pH= (不考虑溶液体积的变化)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com