
【题目】当0.01mol氯化铬(III)(CrCl3·6H2O)在水溶液中用过量的硝酸银处理时,有0.02mol氯化银沉淀析出,此样品的配离子的表示式为
A. [Cr(H2O)6]3+ B. [CrCl(H2O)5]2+ C. [CrCl2(H2O)4]+ D. [CrCl3(H2O)3]
科目:高中化学 来源: 题型:
【题目】下列有关1molNaOH的说法中,正确的是
A. NaOH的摩尔质量为40g
B. 1mol NaOH 的质量为40g/mol
C. 标准状况下,1molNaOH 所占的体积为22.4L
D. 将1molNaOH溶于水配成100mL溶液,则溶液中溶质的物质的量浓度为10mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式与所述事实相符且正确的是( )
A. 实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓)![]() Mn2++2Cl﹣+Cl2↑+2H2O
Mn2++2Cl﹣+Cl2↑+2H2O
B. Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C. 向NaHSO4溶液中滴加Ba(OH)2溶液至呈中性:2H++SO42﹣+Ba2++2OH﹣=2H2O+BaSO4↓
D. 向次氯酸钠溶液中通入SO2:2ClO+SO2+H2O=SO32-+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 元素的电负性越大,其单质越稳定
B. 分子晶体中可能不存在共价键
C. 晶格能越大,形成的离子晶体越稳定
D. 金属晶体和离子晶体均具有延展性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选用金属材料时,以下方面需要考虑的是( ) ①主要用途 ②物理性质、化学性质 ③价格 ④加工难度 ⑤日常维护 ⑥环境保护
A.①②③
B.③④⑤
C.①⑤⑥
D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,且为18电子微粒;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如图所示(某些条件已略去)。请用化学用语回答下列问题:

(1)A在元素周期表中的位置
A、B单质对应元素的简单离子半径由大到小的顺序为 。
(2)丙的电子式为 ,丁中所包含的化学键类型有 (填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(3)甲和水反应生成戊和丙的化学方程式为 。
(4)一定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC)。已知该反应生成1mol乙时放出536kJ热量,其热化学方程式为 。
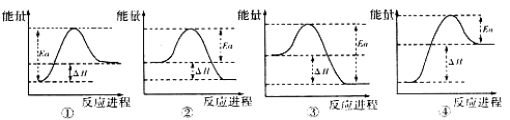
(5)已知另有物质己为中学常见黑色磁性氧化物,能够与A在一定条件下发生反应,实验测得与A反应的焓变(△H)和活化能(Ea)。下列能量关系图合理的是 (填写序号)。
(6)资料显示物质己可用于除去地下水中的TcO4— (99Tc具有放射性)。在弱酸性条件下,物质己将TcO4— 转化为难溶于水的TcO2,同时得到一种难溶于水的弱碱,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯铁的熔点为1 535 ℃,在高炉中炼铁时,生铁(含碳量较高的合金)在1 200 ℃左右就熔化了,这是因为( )
A.铁的纯度越高熔点越低
B.合金的熔点比其成分物质的熔点高
C.合金的熔点比其成分物质的熔点低
D.在高炉中熔化的过程中发生了化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“4.14玉树地震”后,消毒尤为重要,其中常用的消毒剂为“84”消毒液,市场上销售的“84”消毒液,其商品标识上有如下叙述: ①本品为无色溶液,呈碱性 ②使用时加水稀释 ③可对餐具、衣物进行消毒,可漂白浅色衣服 则其有效成份可能是
A.Cl2 B.SO2 C.NaClO D.KMnO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com