
| A. | 硫元素被氧化 | B. | O2失去电子 | ||
| C. | CuS仅作还原剂 | D. | 反应中Cu元素化合价没有发生变化 |
分析 A.化合价升高的元素失去电子被氧化;
B.化合价降低的元素得到电子;
C.还原剂是元素化合价升高的物质;氧化剂是元素化合价降低的物质;
D.Cu2S 在反应中,铜元素化合价从+1价变化降低为0价.
解答 解:A.在该反应中S元素的化合价由反应前Cu2S中的-2价变为反应后SO2中的+4价,化合价升高,失去电子,硫元素被氧化,故A正确;
B.O2中氧元素的化合价由反应前O2的0价变为反应后SO2的-2价,化合价降低,得到电子,故B错误;
C.Cu2S 在反应中,铜元素化合价从+1价变化降低为0价,硫元素化合价从-2价升高到+4价;所以Cu2S 在反应中做氧化剂和还原剂,故C错误;
D.Cu2S 在反应中,铜元素化合价从+1价变化降低为0价,则Cu元素化合价降低,获得电子,被还原,故D错误;
故选A.
点评 本题考查了氧化还原反应的概念分析判断,关键是判断反应前后元素化合价变化,题目难度不大.


 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:选择题
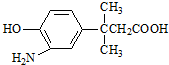 的表述不正确的是( )
的表述不正确的是( )| A. | 该物质能发生缩聚反应 | |
| B. | 该物质的核磁共振氢谱上共有7个峰 | |
| C. | 该物质遇FeCl3溶液显色 | |
| D. | 1 mol该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为2:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成1 mol N2,电子转移总数为3NA | B. | 生成1 mol N2,电子转移总数为5NA | ||
| C. | 溶解1 mol Zn,电子转移总数为2NA | D. | 溶解1 mol Zn,电子转移总数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
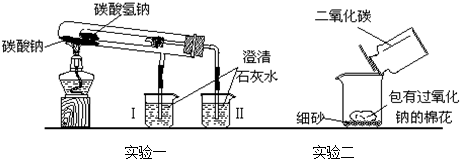
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
| H2 | HCl | Cl2 | ClF |
| 两个原子的s轨道重叠 | 氢原子的s轨道和氯原子的p轨道重叠 | 一个氯原子的s轨道和另一个氯原子的p轨道重叠 | 氯原子的p轨道和氟原子的p轨道重叠 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴入适量AgNO3溶液和稀硝酸,观察到有白色沉淀 | |
| B. | 滴入适量FeCl3溶液,溶液变黄,但无沉淀生成 | |
| C. | 测得反应后溶液中Na+与Cl-的个数比为1:1 | |
| D. | 滴入几滴酚酞试液,酚酞试液不变色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与水反应时增大水的用量 | |
| B. | Fe与稀硫酸反应制取氢气时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,增大压强 | |
| D. | 将铝片改为铝粉,做铝与氧气反应的实验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com