
分析 反应前后固体减少的质量为生成氧气的质量,据此计算出生成氧气的质量;然后根据反应2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑计算出分解的高锰酸钾的质量,然后计算出高锰酸钾的分解率.
解答 解:设反应分解的KMnO4的质量为x,
反应前后固体减少的质量为生成氧气的质量,则反应产生O2的质量为:10g-9.2g=0.8g;
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 0.8g
则:$\frac{316}{x}$=$\frac{32}{0.8}$,
解得:x=7.9g,
则高锰酸钾的分解率为:$\frac{7.9g}{10g}$×100%=79%,
答:反应生成氧气的质量是0.8g,高锰酸钾的分解率是79%.
点评 本题考查了化学方程式的计算,题目难度不大,明确发生反应的原理为解答关键,注意掌握分解率的概念及表达式,试题侧重基础知识的考查,有利于提高学生的化学计算能力.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | SO3 | B. | PCl3 | C. | NO3- | D. | BCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
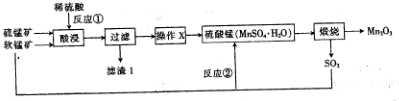
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
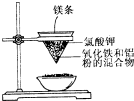 用如图所示的装置进行实验,回答下列问题:
用如图所示的装置进行实验,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
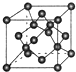 现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期,B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:
现有A、B、C、D、E、F原子序数依次增大的六种元素,它们位于元素周期表的前四周期,B元素含有3个能级,且每个能级所含的电子数相同;D的原子核外有8个运动状态不同的电子;E元素与F元素处于同一周期相邻的族,它们的原子序数相差3,且E元素的基态原子有4个未成对电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用纯碱制烧碱 2KOH+Na2CO3=K2CO3+2NaOH 复分解反应 | |
| B. | 我国古代的“湿法炼铜”:2Fe+3CuSO4=3Cu+Fe2(SO4)3置换反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 证明金属镁的活动性比铁强:3Mg+2Fe(OH)3=3Mg(OH)2+2Fe 置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com