
已知![]() +CO2+H2O→
+CO2+H2O→![]() +NaHCO3,某有机物的结构简式为:
+NaHCO3,某有机物的结构简式为: ,Na、NaOH、NaHCO3分别与等物质的量的该有机物恰好反应时,消耗Na、NaOH、NaHCO3的物质的量之比为( )
,Na、NaOH、NaHCO3分别与等物质的量的该有机物恰好反应时,消耗Na、NaOH、NaHCO3的物质的量之比为( )
A.3∶3∶2 B.3∶2∶1 C.1∶1∶1 D.3∶2∶2
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 温度/℃ | 800 | 1000 | 1200 | 1400 |
| 平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
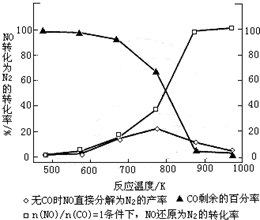
| n(NO) |
| n(CO) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中所有原子在同一平面内 | B、分子中不含氢原子 | C、在ABn型分子中,A元素为最高正价 | D、在ABn型分子中,A原子最外层电子均已成键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com