(2012?泰州二模)乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇的一种反应原理为:
2CO(g)+4H
2(g)?CH
3CH
2OH(g)+H
2O(g)△H=-256.1kJ?mol
-1.
已知:H
2O(l)=H
2O(g)△H=+44kJ?mol
-1CO(g)+H
2O(g)?CO
2(g)+H
2(g)△H=-41.2kJ?mol
-1(1)以CO
2(g)与H
2(g)为原料也可合成乙醇,其热化学方程式如下:
2CO
2(g)+6H
2(g)?CH
3CH
2OH(g)+3H
2O(l)△H=
-305.7 kJ?mol-1
-305.7 kJ?mol-1
.
(2)CH
4和H
2O(g)在催化剂表面发生反应CH
4+H
2O?CO+3H
2,该反应在不同温度下的化学平衡常数如下表:
| 温度/℃ |
800 |
1000 |
1200 |
1400 |
| 平衡常数 |
0.45 |
1.92 |
276.5 |
1771.5 |
①该反应是
吸热
吸热
反应(填“吸热”或“放热”);
②T℃时,向1L密闭容器中投入1molCH
4和1mol H
2O(g),平衡时c(CH
4)=0.5mol?L
-1,该温度下反应CH
4+H
2O?CO+3H
2的平衡常数K=
6.75
6.75
.
(3)汽车使用乙醇汽油并不能减少NO
x的排放,这使NO
x的有效消除成为环保领域的重要课题.某研究小组在实验室以Ag-ZSM-5为催化剂,测得NO转化为N
2的转化率随温度变化情况如下图.
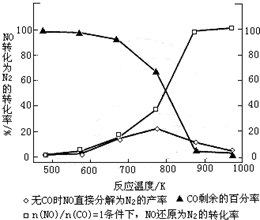
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为
该反应是放热反应,升高温度反应更有利于向逆反应方向进行
该反应是放热反应,升高温度反应更有利于向逆反应方向进行
;在
=1的条件下,应控制的最佳温度在
870℃
870℃
左右.
②用C
xH
y(烃)催化还原NO
x也可消除氮氧化物的污染.写出CH
4与NO
2发生反应的化学方程式:
CH4+2NO2→CO2+N2+2H2O
CH4+2NO2→CO2+N2+2H2O
.
(4)乙醇-空气燃料电池中使用的电解质是搀杂了Y
2O
3的ZrO
2晶体,它在高温下能传导O
2-离子.该电池负极的电极反应式为
CH3CH2OH-12e-+6O2-=2CO2+3H2O
CH3CH2OH-12e-+6O2-=2CO2+3H2O
.



