
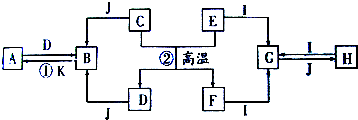
| T(℃) | 200 | 600 | 800 |
| ρ(g/L) | 6.881 | 2.650 | 1.517 |
| 气体摩尔体积(L/mol) | 38.8 | 71.6 | 88.0 |
| ||
| ||
| 3.9g |
| 78g/mol |
| 186.9 |
| 133.5 |


科目:高中化学 来源: 题型:
| A、汽油是纯净物,乙醇汽油是混合物 |
| B、诗句“春蚕到死丝方尽,蜡炬成灰泪始干”中的“丝”和“泪”分别是蛋白质和烃 |
| C、糖类、蛋白质在一定条件下都能发生水解反应 |
| D、乙烯、植物油和苯都能与氢气发生加成反应,是因为其结构中都含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
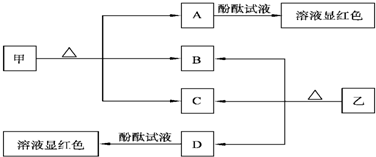
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
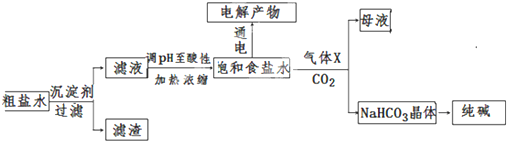
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
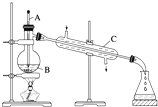 选择下列实验方法分离物质,将分离方法的序号填在横线上.
选择下列实验方法分离物质,将分离方法的序号填在横线上.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com