
【题目】1834年,德国科学家米希尔里希通过蒸馏安息香酸(苯甲酸)和石灰的混合物得到一种液体物质,将其命名为苯。
(1)分子式为C6H6的有机化合物有多种同分异构体。写出符合下列条件的苯的同分异构体。
①分子式为C6H6,含有一个叁键,其余为双键,且叁键、双键均不相邻的无支链的结构简式:__________________________(写一个即可,下同)。
②分子式为C6H6,含有2个四元环的结构简式__________________________________。
③分子式为C6H6,含有多元环的结构简式_____________________________________。
(2)苯乙烯在常温下用镍做催化剂与氢气加成得到乙苯,很难得到乙基环已烷,这说明:___________________________________________________。
(3)1866年凯库勒提出了苯的单键、双键 交替的正六边形平面结构,解释了苯的部分性质。请你用一些事实说明:苯环上的化学键不是一般的碳碳单键和碳碳双键,而是介于一种碳碳单键和碳碳双键之间的特殊键。如:__________,__________,_____________,(至少填3 种不同类的事实)。
(4)甲苯是苯的同系物。写出下列反应的化学方程式:
①甲苯与溴单质在光照条件下发生反应______________________;
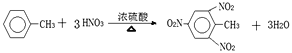
②甲苯与混酸发生硝化反应_________________________。
【答案】 CH≡C-CH=CH-CH=CH2或 CH2=CH-C≡C-CH=CH2 ![]() 或
或![]()
![]() 苯环中的碳碳键比碳碳双键稳定的多 不能与溴水发生加成反应 不能与酸性的高锰酸钾发生氧化反应(不能使高锰酸钾褪色) 邻二卤代物不存在异构体或环中的碳碳键都相同
苯环中的碳碳键比碳碳双键稳定的多 不能与溴水发生加成反应 不能与酸性的高锰酸钾发生氧化反应(不能使高锰酸钾褪色) 邻二卤代物不存在异构体或环中的碳碳键都相同 ![]()
【解析】(1)①C6H6的不饱和度为![]() =4,含有一个叁键,其余为双键,则含有2个双键,叁键、双键均不相邻的无支链的结构简式为CH≡C-CH=CH-CH=CH2或 CH2=CH-C≡C-CH=CH2,故答案为:CH≡C-CH=CH-CH=CH2或 CH2=CH-C≡C-CH=CH2;
=4,含有一个叁键,其余为双键,则含有2个双键,叁键、双键均不相邻的无支链的结构简式为CH≡C-CH=CH-CH=CH2或 CH2=CH-C≡C-CH=CH2,故答案为:CH≡C-CH=CH-CH=CH2或 CH2=CH-C≡C-CH=CH2;
②C6H6的不饱和度为![]() =4,含有2个四元环,同时含有2个双键或1个三键,满足条件的结构简式有
=4,含有2个四元环,同时含有2个双键或1个三键,满足条件的结构简式有![]() 或
或![]() ,故答案为:
,故答案为:![]() 或
或![]() ;
;
③C6H6的不饱和度为![]() =4,含有多元环的结构简式有
=4,含有多元环的结构简式有![]() ,故答案为:
,故答案为:![]() ;
;
(2)苯乙烯在常温下用镍做催化剂与氢气加成得到乙苯,很难得到乙基环已烷,这说明苯环中的碳碳键比碳碳双键稳定,故答案为:苯环中的碳碳键比碳碳双键稳定的多;
(3)苯不能与溴水发生加成反应,不能与酸性的高锰酸钾发生氧化反应(不能使高锰酸钾褪色),邻二卤代物不存在异构体或环中的碳碳键都相同,说明苯环上的化学键不是一般的碳碳单键和碳碳双键,而是介于一种碳碳单键和碳碳双键之间的特殊键,故答案为:不能与溴水发生加成反应;不能与酸性的高锰酸钾发生氧化反应(不能使高锰酸钾褪色);邻二卤代物不存在异构体或环中的碳碳键都相同;
(4)①甲苯与溴单质在光照条件下发生侧链的取代反应,反应的化学方程式为![]() ,故答案为:
,故答案为:![]() ;
;
②甲苯与混酸发生甲基邻位和对位的硝化反应,反应的方程式为 ,故答案为:
,故答案为: 。
。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】塑料废弃物又称“白色污染”,它的危害有
① 难以分解,破坏土壤结构,影响植物生长 ② 污染海洋 ③ 危及海洋生物的生存 ④ 破坏环境卫生,污染地下水
A. ①②③ B. ①③④ C. ②③④ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,将a g NH3完全溶于水,得到V mL溶液,设该溶液的密度为ρ g·cm-3,质量分数为ω,其中含N的物质的量为b mol。下列叙述中不正确的是
A. 溶质的质量分数ω=![]() ×100%
×100%
B. 溶质的物质的量浓度c= 1000a/17Vmol·L-1
C. 溶液中c(OH-)= 1000b/Vmol·L-1+c(H+)
D. 上述溶液中再加入V mL水后,所得溶液中溶质的质量分数小于0.5ω
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶“威露士”ke牌“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO、1 000 mL、密度1.192 g·cm3,稀释100倍(体积比)后使用。请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为________mol·L1。
(2)该同学取100 mL“威露士”牌“84消毒液”稀释后用于消毒,稀释后的溶液中c(Na+)=________mol·L1。
(3)一瓶“威露士”牌“84消毒液”能吸收空气中________L的CO2(标准状况)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)
(4)该同学参阅“威露士”牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25%NaClO的消毒液。下列说法正确的是________。
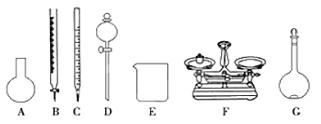
A.如上图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制
C.利用购买的商品NaClO来配制可能导致结果偏低
D.需要称量的NaClO固体质量为143 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是

A. 汉黄芩素的分子式为C16H14O5
B. 该物质遇FeCl3溶液显色
C. 1 mol该物质与溴水反应,最多消耗1 mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2Y2-是乙二胺四乙酸根(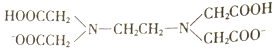 )的简写,可与多种金属离子形成络合物。
)的简写,可与多种金属离子形成络合物。
I. H2Y2-与Fe2+形成的络合物FeY2-可用于吸收烟气中的NO。其吸收原理:
FeY2-(aq)+NO(g)![]() FeY2-(NO)(aq) △H<0
FeY2-(NO)(aq) △H<0
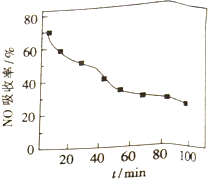
(1)将含NO的烟气以一定的流速通入起始温度为50℃的FeY2-溶液中。NO吸收率随通入烟气的时间变化如右图。时间越长,NO吸收率越低的原因是_________。
(2)生成的FeY2-(NO)(aq)可通过加入铁粉还原再生,其原理:FeY2-(NO)(aq)+Fe+H2O→FeY2-(aq)+Fe(OH)2+NH3(未配平)。
若吸收液再生消耗14g铁粉,则所吸收的烟气中含有NO的物质的量为_______。
II.络合铜(CuY2-)废水的处理一直是环境工程领域的研究热点。
(1)H2Y2-与Cu2+、Fe3+、Ca2+络合情况如下表:
络合反应 | lgK(K为平衡常数) |
Cu2++H2Y2- | 18.8 |
Fe3++H2Y2- | 25.1 |
Ca2++H2Y2- | 10.7 |
①表中最不稳定的金属络合物是_____(填化学式)。向含有络合铜(CuY2-)废水中加入一种黄色的盐溶液A可解离出Cu2+,则盐A中阳离子为________(填化学式)。
②调节pH可将解离出的Cu2+转化为Cu(OH)2沉淀,若要使c(Cu2+)≤2.2×10-4mol/L,pH应不低于________(常温下Ksp[Cu(OH)2]= 2.2×10-20)。
(2)羟基自由基(-OH)、Na2FeO2都可氧化络合铜中的Y4-而使Cu2+得到解离。
①酸性条件下,-OH可将Y4-(C10H12O8N24-)氧化生成CO2、H2O、N2。该反应的离子方程式为___________________。
②Na2FeO4在酸性条件下不稳定。用Na2FeO4处理后的废水中Cu2+的浓度与pH的关系如右图。pH越大,/span>废水处理效果越好,这是因为______________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池式氧传感器原理构造如图,可测定O2的含量。工作时铅极表面会逐渐附着Pb(OH)2。下列说法不正确的是

A. Pt电极上发生还原反应
B. 随着使用,电解液的pH逐渐减小
C. a ×10-3molO2反应,理论上可使Pb电极增重68a mg
D. Pb电极上的反应式为Pb+2OH--2e-=Pb(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在已达到电离平衡的0.1 mol/L的醋酸溶液中,欲使平衡向电离的方向移动,同时使溶液的pH降低,应采取的措施是( )
A. 加少量盐酸
B. 加热
C. 加少量醋酸钠晶体
D. 加少量NaOH晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com