
【题目】“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶“威露士”ke牌“84消毒液”,并查阅相关资料和消毒液包装说明得到如下信息:“84消毒液”:含25%NaClO、1 000 mL、密度1.192 g·cm3,稀释100倍(体积比)后使用。请根据以上信息和相关知识回答下列问题:
(1)该“84消毒液”的物质的量浓度为________mol·L1。
(2)该同学取100 mL“威露士”牌“84消毒液”稀释后用于消毒,稀释后的溶液中c(Na+)=________mol·L1。
(3)一瓶“威露士”牌“84消毒液”能吸收空气中________L的CO2(标准状况)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)
(4)该同学参阅“威露士”牌“84消毒液”的配方,欲用NaClO固体配制480 mL含25%NaClO的消毒液。下列说法正确的是________。
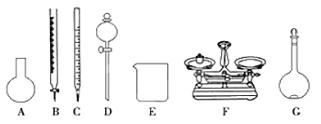
A.如上图所示的仪器中,有四种是不需要的,还需一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干才能用于溶液配制
C.利用购买的商品NaClO来配制可能导致结果偏低
D.需要称量的NaClO固体质量为143 g
【答案】4 0.04 89.6 C
【解析】
(1)根据含25%NaClO、1 000 mL 、密度1.192 g·cm3,及根据c=1000![]() w/M来计算;(2)根据稀释前后溶质的物质的量不变来计算;(3)根据反应CO2+NaClO+H2O=NaHCO3+HClO来计算;(4)根据溶液的配制及c=n/V、m=nM来分析即可。
w/M来计算;(2)根据稀释前后溶质的物质的量不变来计算;(3)根据反应CO2+NaClO+H2O=NaHCO3+HClO来计算;(4)根据溶液的配制及c=n/V、m=nM来分析即可。
(1)根据c=1000![]() w/M,则c(NaClO)=(1000mL
w/M,则c(NaClO)=(1000mL![]() 1.192g·cm3
1.192g·cm3![]() 25%)/(1L
25%)/(1L![]() 74.5 g·mol1)=4.0 mol·L1 ,因此答案是:4.0;
74.5 g·mol1)=4.0 mol·L1 ,因此答案是:4.0;
(2)根据稀释前后溶质的物质的量不变,则100mL![]() 4.0 mol·L1/10000=0.04 mol·L1, 稀释100倍c(Na+)=0.04mol·L1,答案:0.04。
4.0 mol·L1/10000=0.04 mol·L1, 稀释100倍c(Na+)=0.04mol·L1,答案:0.04。
(3)一瓶“84消毒液”含有n(NaClO)=1L![]() 4.0 mol·L1=4 mol
4.0 mol·L1=4 mol
根据反应CO2+NaClO+H2O=NaHCO3+HClO,则需要CO2的物质的量为n(NaClO)=4.0 mol即标准状况下V(CO2)= 4 mol ![]() 22.4L/mol=89.6L,因此答案是:89.6;
22.4L/mol=89.6L,因此答案是:89.6;
(4)A、需用托盘天平称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量瓶和胶头滴管来定容,图示的A、B、C、D不需要,但还需玻璃棒和胶头滴管,故A错误;B、配制过程中需要加入水,所以经洗涤干净的容量瓶不必烘干后再使用,故B错误;C、因为NaClO易吸收空气中的H2O、CO2而变质,所以商品NaClO可能部分变质导致NaClO减少,配制的溶液中溶质的物质的量减小,结果偏低,所以C选项是正确的;D、应选取500mL的容量瓶进行配制,然后取出480mL即可,所以需要NaClO的质量:0.5L![]() 4.0 mol·L1
4.0 mol·L1 ![]() 74.5 g·mol1=149g,故D错误;答案是:C。
74.5 g·mol1=149g,故D错误;答案是:C。


科目:高中化学 来源: 题型:
【题目】(一)铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表中第___族,其基态原子中未成对电子的个数为_________。
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为_________,尿素分子中C、N原子的杂化方式分别是_____、___,其分子中σ键与π键的数目之比为___,所含非金属元素的电负性由大到小的顺序是_______。
(二)已知元素镓和砷的单质及其化合物在工业生产上有重要的用途。回答下列问题:
(1)砷元素基态原子的电子排布式为_____________。
(2)砷与氢元素。可形成化合物砷化氢,该化合物的空间构型为_____,其中砷原子的杂化方式为__________。
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柔红酮是一种医药中间体,其结构简式如图所示。下列说法正确的是( )
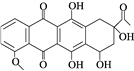
A. 每个柔红酮分子中含有2个手性碳原子
B. 柔红酮分子中所有的碳原子都在同一个平面上
C. 1 mol柔红酮最多可与2 mol Br2发生取代反应
D. 一定条件下柔红酮可发生氧化、加成、消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)从氯化钾溶液中得到氯化钾固体,选择装置___(填代表装置图的字母,下同);除去自来水中的Cl﹣等杂质,选择装置___。
(2)从碘水中分离出I2,选择装置____,该分离方法的名称为____。
(3)装置A中①的名称是_____,进水的方向是从_____口(填“上”或“下”)进水。装置B在分液时为使液体顺利滴下,除打开漏斗下端的旋塞外,还应进行的具体操作是______。
(4)粗盐中含Ca2+、Mg2+、Fe3+、SO42﹣等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④过滤 ⑤溶解 ⑥加盐酸调节溶液的pH等于7 ⑦蒸发,操作顺序合理的是_____(选填项字母)
a.⑤②③①④⑥⑦ b.⑤①②③④⑥⑦ c.⑤②①③⑥④⑦ d.⑤③②①④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1834年,德国科学家米希尔里希通过蒸馏安息香酸(苯甲酸)和石灰的混合物得到一种液体物质,将其命名为苯。
(1)分子式为C6H6的有机化合物有多种同分异构体。写出符合下列条件的苯的同分异构体。
①分子式为C6H6,含有一个叁键,其余为双键,且叁键、双键均不相邻的无支链的结构简式:__________________________(写一个即可,下同)。
②分子式为C6H6,含有2个四元环的结构简式__________________________________。
③分子式为C6H6,含有多元环的结构简式_____________________________________。
(2)苯乙烯在常温下用镍做催化剂与氢气加成得到乙苯,很难得到乙基环已烷,这说明:___________________________________________________。
(3)1866年凯库勒提出了苯的单键、双键 交替的正六边形平面结构,解释了苯的部分性质。请你用一些事实说明:苯环上的化学键不是一般的碳碳单键和碳碳双键,而是介于一种碳碳单键和碳碳双键之间的特殊键。如:__________,__________,_____________,(至少填3 种不同类的事实)。
(4)甲苯是苯的同系物。写出下列反应的化学方程式:
①甲苯与溴单质在光照条件下发生反应______________________;
②甲苯与混酸发生硝化反应_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是( )
A. 主族元素的电负性越大,元素原子的第一电离能一定越大
B. 在元素周期表中,元素电负性从左到右越来越大
C. 金属元素电负性一定小于非金属元素电负性
D. 在形成化合物时,电负性越小的元素越容易显示正价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族化合物A(C9H12O)常用于药物及香料的合成,A有如下转化关系:
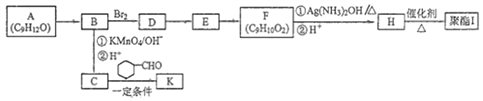
已知:
①A的苯环上只有一个支链,支链上有两种不同环境的氢原子
②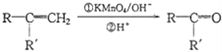 +CO2
+CO2
③RCOCH3+R'CHO![]() RCOCH=CHR'+H2O
RCOCH=CHR'+H2O
回答下列问题:
(1)A生成B的反应类型为__________,由D生成E的反应条件为_______________。
(2)H中含有的官能团名称为______________。
(3)I的结构简式为__________________________。
(4)由E生成F的化学方程式为____________________________________________。
(5)F有多种同分异构体,写出一种符合下列条件的同分异构体的结构简式为:___________________。
①能发生水解反应和银镜反应
②属于芳香族化合物且分子中只有一个甲基
③具有5组核磁共振氢谱峰
(6)糠叉丙酮(![]() )是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇[(CH3)3COH]和糠醛(
)是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇[(CH3)3COH]和糠醛(![]() )为原料制备糠叉丙酮的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):___________________。
)为原料制备糠叉丙酮的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com