
【题目】如图所示是分离混合物时常用的仪器、从左到右,可以进行的混合物操作分别是
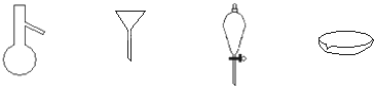
A.蒸馏、蒸发、萃取、过滤
B.蒸馏、过滤、萃取、蒸发
C.萃取、过滤、蒸馏、蒸发
D.过滤、蒸发、萃取、蒸馏
【答案】B
【解析】蒸馏烧瓶用于分离沸点相差较大的两种液体的分离或难挥发性固体和液体的分离,即蒸馏;普通漏斗用于分离互不相溶的固体和液体,即过滤;分液漏斗用来分离互不相溶的液体或用来分离在不同溶剂中溶解度不同的混合物,即分液或萃取;蒸发皿用于可溶性固体和液体的分离,即蒸发,所以从左至右,可以进行的混合物分离操作分别是:蒸馏、过滤、分液或萃取、蒸发,故选B。
【规律总结】要结合混合物的组分性质选择分离方式;常见物质分离与提纯方法小结:
方法 | 适用范围 | 主要仪器 | 注意点 | 实例 | |
固+液 | 蒸发 | 易溶固体与液体分开 | 酒精灯、蒸发皿、玻璃棒 | ①不断搅拌;②最后用余热加热;③液体不超过容积2/3 | NaCl(H2O) |
固+固 | 结晶 | 溶解度差别大的溶质分开 | NaCl(KNO3) | ||
升华 | 能升华固体与不升华物分开 | 酒精灯 | I2(NaCl) | ||
固+液 | 过滤 | 易溶物与难溶物分开 | 漏斗、烧杯 | ①一贴、二低、三靠;②沉淀要洗涤;③定量实验要“无损” | NaCl(CaCO3) Fe粉(Al粉) |
液+液 | 萃取 | 溶质在互不相溶的溶剂里,溶解度的不同,把溶质分离出来 | 分液漏斗 | ①先查漏;②对萃取剂的要求;③使漏斗内外大气相通;④上层液体从上口倒出 | 从溴水中提取Br |
分液 | 分离互不相溶液体 | 分液漏斗 | 乙酸乙酯与饱和Na2CO3溶液 | ||
蒸馏 | 分离沸点不同混合溶液 | 蒸馏烧瓶、冷凝管、温度计、牛角管 | ①温度计水银球位于支管处;②冷凝水从下口通入;③加碎瓷片 | 乙醇和水、 I2和CCl4 |


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:
【题目】有机物G(1,4-环己二醇)是重要的医药中间体和新材料单体,可通过以下流程制备。

完成下列填空:
(1)写出C中含氧官能团名称_____________。
(2)判断反应类型:反应①_______________;反应③_________________。
(3)写出B的结构简式 _____________________。
(4)一定条件下D脱氢反应得一种产物,化学性质比较稳定,易取代、难加成。该产物属于_________(填有机物类别),说明该物质中碳碳键的特点____________________________。
(5)1,3-丁二烯是应用广泛的有机化工原料,它是合成D的原料之一,它还可以用来合成氯丁橡胶(![]() )。写出以1,3-丁二烯为原料制备氯丁橡胶的单体的合成路线。_________________
)。写出以1,3-丁二烯为原料制备氯丁橡胶的单体的合成路线。_________________
(合成路线常用的表示方式为:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氯化二硫(S2C12)是工业上常用的硫化剂。常温下是一种液体,沸点137℃,易与水反应。实验室可通过硫与少量氯气在110140℃反应制得S2Cl2粗品,氯气过量则会生成SCl2。
(1)选取以下装置制取少量S2Cl2:

①仪器m的名称为_____________。
②装置连接顺序:A→________________________________→E→D。
③A中发生反应的离子方程式为 _________________________。
④装置F的作用是____________________。
⑤D中的最佳试剂是__________(填标号)。
a.碱石灰 b.浓硫酸 c.无水氯化钙
⑥为了提高S2Cl2的纯度,关键的是控制好温度和_______________________。
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如下实验方案来测定该混合物的SO2的体积分数。

①W溶液可以是下列溶液中的__________(填标号);
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为__________(含V、m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(10分)金属镍及其化合物在合金材料以及催化剂等方面应用广泛。
(1)基态镍原子的外围电子排布式为 。
(2)金属镍能与CO形成配合物Ni(CO)4,写出与CO互为等电子体的一种分子和一种离子的化学式 、 。
(3)很多不饱和有机物在Ni催化下可与H2发生加成反应。
如①CH2=CH2、②HC≡CH、③![]() 、④HCHO,其中碳原子采取sp2杂化的分子有
、④HCHO,其中碳原子采取sp2杂化的分子有
(填物质序号),HCHO分子的立体结构为 形。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为 。

(5)丁二酮肟常用于检验Ni2+:在稀氨水中,丁二酮肟与Ni2+反应生成鲜红色沉淀,其结构如上右图所示。该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气系统中的催化转化器,可有效降低尾气中的CO、NO和NO2等向大气排放。在催化转化器的前半部发生的反应为2CO(g) + 2NO(g) ![]() 2CO2(g) + N2(g)。下列说法能充分说明该反应已经达到化学平衡状态的是
2CO2(g) + N2(g)。下列说法能充分说明该反应已经达到化学平衡状态的是
A. CO的转化率100% B. CO、NO、CO2、N2的浓度相等
C. CO、NO、CO2、N2在容器中共存 D. CO、NO、CO2、N2的浓度均不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)关注营养平衡,合理使用药物,有利于身心健康,现有下列四种物质:
A、麻黄碱 B、西红柿 C、青霉素 D、阿司匹林
①富含维生素的是________;
②用于治疗哮喘、鼻粘膜充血引起的鼻塞等,但属于国际奥委会严格禁止的兴奋剂的是_________;
③用作抗生素,在使用时需要进行皮肤敏感实验的是________;
④能起镇热解痛作用的是_______ ;
(2)化学是材料科学发展的基础,合理使用材料有利于人类的生产和生活。
①下列物质中含有机高分子材料的是_________________ ;
A、汽车轮胎 B、陶瓷 C、玻璃
②下列防止钢铁锈蚀的措施不合理的是____________;
A.铁质篮球架刷油漆
B.改变金属内部结构制成不锈钢.
C.在地下钢铁管道上连接铜块
③某学生欲探究在NaCl溶液、蒸馏水和空气中铁锈蚀的快慢,设计了如下实验。一周后,实验序号为__________的试管中铁钉锈蚀速度最快。
实验序号 | A | B | C |
实验 内容 |
|
|
|
随着工业发展和社会的进步,人们日益关注环境污染问题。
①下列属于室内空气污染的是____________ (填字母);
A.CO2 B.甲醛 C.N2
②按照垃圾分类的方法,易拉罐瓶属于_______________(填“可回收物”或“可堆肥垃圾”);
③工业废水需处理达标后才能排放。下列废水处理的方法合理的是_______;
A.用氯气除去废水中的悬浮物
B.用中和法除去废水中的酸
C.用混凝剂(如:明矾)除去废水中的重金属离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如下图所示(某些条件和部分产物已略去)。下列说法不正确的是

A. 若甲既能与盐酸反应又能与NaOH溶液反应则丙可能属于两性氧化物
B. 若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙只能为Na2O2
C. 若丙、丁混合产生白烟,且丙为18电子分子,丁为10电子分子,则乙的水溶液可能具有漂白作用
D. 若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序可能为甲<丙<戊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4mol A气体和2mol B气体在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法:
2C(g),若经2s后测得C的浓度为0.6mol·L-1,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol·L-1
其中正确的是
A.①③ B.①④ C.②③ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组设计如下图装置研究电化学原理,下列说法中错误的是

A. 若开始时开关K与a连接,其反应与铁的吸氧腐蚀类似
B. 若开始时开关K与b连接,则标准状况下B极产生2.24 L气体,转移电子0.2 mol
C. 若开始时开关K与b连接,则该装置是化学能转变为电能
D. 若开始时开关K与b连接,其原理类似于钢铁防护中外加电流的阴极保护法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com