
【题目】NaCl晶体中Na+与Cl-都是等距离交错排列,若食盐的密度是2.2 g·cm-3,阿伏加德罗常数6.02×1023mol-1,食盐的摩尔质量为58.5 g·mol-1。则食盐晶体中两个距离最近的钠离子中心间的距离是多少?_______
【答案】两个距离最近的Na+中心间的距离d=![]() a=4.0×10-8cm。
a=4.0×10-8cm。
【解析】
从上述NaCl晶体结构模型中分割出一个小立方体,如图中所示:其中a代表其边长,d代表两个距离最近的Na+中心间的距离,利用“均摊法”计算小立方体中Na+、Cl-的数目,进而计算小立方体的质量,根据公式密度![]() 计算出小立方体的边长,进而计算两个距离最近的钠离子中心间的距离。
计算出小立方体的边长,进而计算两个距离最近的钠离子中心间的距离。
从上述NaCl晶体结构模型中分割出一个小立方体,如图中所示:其中a代表其边长,d代表两个Na+中心间的距离。由此不难想象出小立方体顶点上的每个离子均为8个小立方体所共有。因此小立方体含Na+:4×1/8=1/2,含Cl-:4×1/8=1/2,即每个小立方体含有1/2个(Na+-Cl-)离子对,

每个小立方体的质量![]() ,
,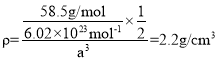
解得:a≈2.81×10-8cm,两个距离最近的Na+中心间的距离d=![]() a≈4.0×10-8cm;
a≈4.0×10-8cm;
故答案为:两个距离最近的Na+中心间的距离为4.0×10-8cm。


科目:高中化学 来源: 题型:
【题目】局部麻醉药普鲁卡因E(结构简式为![]() )的三条合成路线如下图所示(部分反应试剂和条件已省略):
)的三条合成路线如下图所示(部分反应试剂和条件已省略):
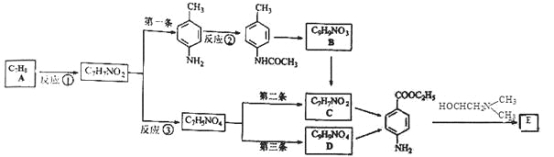
完成下列填空:
(1).比A多一个碳原子,且一溴代物只有3种的A的同系物的名称是___________。
(2).写出反应试剂和反应条件。反应①______;③______
(3).设计反应②的目的是____________。
(4).B的结构简式为_____;C的名称是____。
(5).写出一种满足下列条件的D的同分异构体的结构简式____。
①芳香族化合物 ②能发生水解反应 ③有3种不同环境的氢原子
1 mol该物质与NaOH溶液共热最多消耗_____mol NaOH。
(6).普鲁卡因的三条合成路线中,第一条合成路线与第二条、第三条相比不太理想,理由是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)高温下,C(s)+H2O(g)![]() CO(g)+H2(g) ΔH>0,反应的化学平衡常数表达式K=____ ,该反应随温度升高,K值___(填增大、减小或不变),该反应在高温下自发进行的原因是_____。
CO(g)+H2(g) ΔH>0,反应的化学平衡常数表达式K=____ ,该反应随温度升高,K值___(填增大、减小或不变),该反应在高温下自发进行的原因是_____。
(2)向重铬酸钾溶液中加入氢氧化钠固体,溶液的颜色变化为____,原因是(请从平衡的角度用化学用语及必要的文字说明)____。
(3)密闭容器中充入N2O4达化学平衡,压缩体积达新平衡,整个过程的现象为____。
(4)多元弱酸的逐级电离平衡常数为K1、K2、K3……,则K1、K2、K3的大小关系为___。
(5)1molNO2和1molCO反应生成CO2和NO过程中的能量变化如图,请写出NO2和CO反应的热化学方程式___,向上述可逆反应中加入催化剂,则E1____(填增大、减小或不变,下同);此反应的ΔH____。
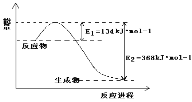
查看答案和解析>>
科目:高中化学 来源: 题型:
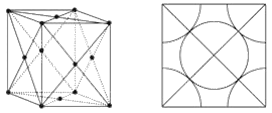
【题目】(1)如图甲所示为二维平面晶体示意图,所表示物质的化学式为AX3的是__________。
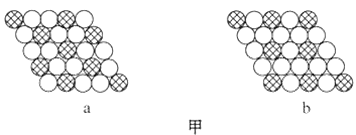
(2)图乙为一个金属铜的晶胞,请完成以下各题。
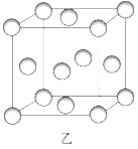
①该晶胞“实际”拥有的铜原子数是_________个。
②该晶胞称为_____________。(填序号)
A.六方晶胞
B.体心立方晶胞
C.面心立方晶胞
③我们在晶体结构中可以划出一块正立方体的结构单元,金属原子处于正立方体的八个顶点和六个侧面上,(图示如下图)这类金属晶体中原子的空间利用率是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,不正确的是
A.过量CO2气体通入NaOH溶液中:CO2+OH-=HCO3-
B.将氯气通入水中:Cl2+H2O![]() Cl-+ClO-+2H+
Cl-+ClO-+2H+
C.向SiO2粉末中加入足量的NaOH溶液:SiO2+2OH-= SiO32-+ H2O
D.用氯化铁溶液腐蚀铜,制作印刷电路板:2Fe3++Cu=2Fe2++Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,关于pH=11的NH3·H2O溶液,下列分析正确的是
A.c(NH3·H2O)=103mol·L1
B.加入少量水,溶液中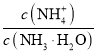 增大
增大
C.由水电离产生的c(OH)=1×1011mol·L1
D.加入等体积pH=3的盐酸,所得溶液:c(Cl)>c(NH4+)>c(H+)>c(OH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某手机电池采用了石墨烯电池,可充电5分钟,通话2小时。一种石墨烯锂硫电池(2Li+S8=Li2S8)工作原理示意图如图。下列有关该电池说法正确的是
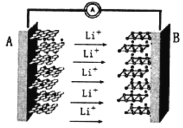
A.A电极为该电源的负极,电极材料主要是金属锂和石墨烯
B.B电极的反应:2Li++S8﹣2e=Li2S8
C.充电时,电极A与电源负极连接,作为阴极
D.为提高电池效率,该电池可选用稀硫酸作为电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,HNO2和CH3COOH的电离常数分別为5.0×10-4和1.7×10-5。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是
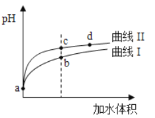
A. 溶液中水的电离程度:b点>c点
B. 曲线Ⅱ代表CH3COOH
C. 相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
D. 从c点到d点,溶液中![]() 保持不变(其中HA、A-分别代表相应的酸和酸根离子)
保持不变(其中HA、A-分别代表相应的酸和酸根离子)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】α-苯基丙烯酸可用于合成人造龙涎香,现以甲苯为原料,按下列方法合成(从F开始有两条合成路线)
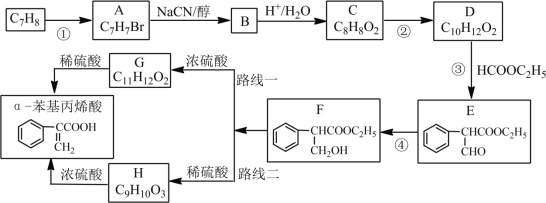
已知:①CH3CH2Br+NaCN![]() CH3CH2CN+NaBr
CH3CH2CN+NaBr
②CH3CH2CN ![]() CH3CH2COOH
CH3CH2COOH
完成下列填空:
(1)写出反应④的反应类型是________反应;写出反应①所需试剂与条件是 _________。
(2)写出C的结构简式:_____________________。
(3)写出一种符合下列条件的F的同分异构体___________________。
①氧原子不与苯环直接相连;②能发生银镜反应;③1mol该物质与足量钠反应产生1mol氢气;④有5种不同氢原子。
(4)检验E是否完全转化为F的方法是_____________________。
(5)路线二与路线一相比不太理想,理由是_______________________。
(6)利用已知条件,设计一条由![]() 制备
制备![]() 的合成路线。___________________________
的合成路线。___________________________
(合成路线的表示方法为![]() )
)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com